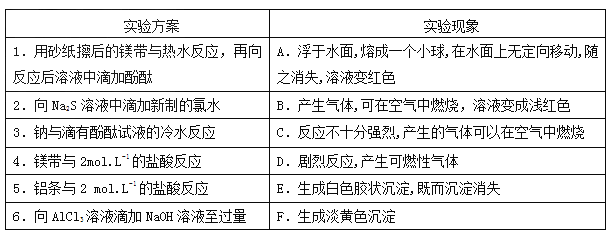
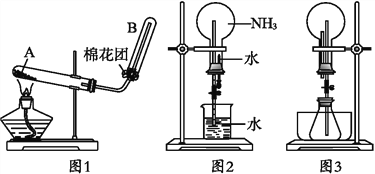
-
下列除去杂质的实验方法不正确的是( )
A. 除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B. 除去Cl2中少量HCl气体:通过饱和食盐水后再干燥气体
C. 除去SiO2中的Al2O3:加入过量氢氧化钠溶液反应后过滤
D. 除去SO2中少量H2O气体:通过浓硫酸除水干燥
难度: 困难查看答案及解析
-
化学无处不在,下列有关“化学与生活”的叙述不正确的是( )
A. 用含硅胶、铁粉的透气小袋与食品一起密封包装
B. 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气
C. CO2、SO2和NO2大量排放,是形成酸雨的根本原因
D. 高空臭氧层能吸收太阳紫外线,保护地球生物,但低空臭氧是污染气体,对生物有危害
难度: 中等查看答案及解析
-
我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿滴,惟玻璃可盛。”这里的“强水”是指( )
A. 氨水 B. 硝酸 C. 醋 D. 卤水
难度: 简单查看答案及解析
-
下列有关物质性质与用途的叙述正确的是( )
A. 浓硫酸具有脱水性,可用作干燥剂
B. NH3极易溶于水,可用作制冷剂
C. 二氧化硫具有漂白性,与氯水混合使用漂白效果更好
D. ClO2具有氧化性,可用于自来水的杀菌消毒
难度: 中等查看答案及解析
-
实际存在的11H、21H、31H 、 H+和H2,它们是( )
A. 氢的五种同位素 B. 五种氢元素
C. 氢的五种核素 D. 氢元素的五种不同微粒
难度: 中等查看答案及解析
-
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是( )
A. 原子最外层电子数:X>Y>Z B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z- D. 原子序数:X>Y>Z
难度: 中等查看答案及解析
-
下列关于物质性质的叙述中正确的是( )
A. (NH4)2S既能与强碱溶液反应,又能与强酸溶液反应
B. N2是大气的主要成分之一,雷雨时,可直接转化为NO2
C. 硫是一种黄色的能溶于水的晶体,既具有氧化性又具有还原性
D. 硅是应用广泛的半导体材料,常温下化学性质活泼
难度: 中等查看答案及解析
-
下列物质的性质比较,正确的是 ( )
A. 气态氢化物稳定性:HF>HCl>H2S B. 碱性:NaOH>KOH>RbOH
C. 还原性强弱: F- > Cl- > Br- > I- D. 酸性:H2SO4>HClO4>HBrO4
难度: 中等查看答案及解析
-
能正确表示下列反应的离子方程式是( )
A. 将Cl2通入氯化亚铁溶液:Fe2++Cl2
Fe3++2Cl-
B. 氯气通入水中:Cl2+H2O
2H++Cl-+ClO-
C. FeCl3溶液中通入过量的氨水: Fe3++3OH-
Fe(OH)3↓
D. Cl2通入烧碱溶液中:Cl2+2OH-
Cl-+ClO-+H2O
难度: 中等查看答案及解析
-
已知X、Y、Z、W(含同一元素)有如下所示转化关系,且X能与W发生反应生成一种易溶于水的盐,则X可能是( )
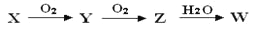 .
.A. N2 B. H2S C. NH3 D. CH4
难度: 中等查看答案及解析
-
X、Y、Z为短周期非金属元素,其相关性质如下:
元素
X
Y
Z
与H2反应条件
暗处反应
光照
高温、催化剂
氢化物水溶液的酸碱性
酸性
酸性
碱性
下列叙述正确的是( )
A. 非金属性:Z<X<Y
B. 气态氢化物稳定性:Z>Y>X
C. 最高价氧化物对应水化物的酸性:X>Z>Y
D. Y、Z的氢化物能反应形成离子化合物
难度: 中等查看答案及解析
-
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
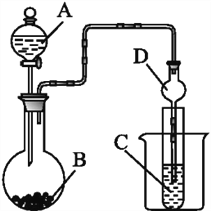
A. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 若A为浓硫酸,B为Na2SO3固体,C中盛紫色石蕊溶液,则C中溶液先变红后褪色
难度: 中等查看答案及解析
-
用下面的方案进行某些离子的检验,其中方案设计严密的是( )
A. 检验试液中的SO42-:试液
无沉淀
白色沉淀
B. 检验试液中的SO32-:试液
气体
褪色
C. 检验试液中的I-:试液
棕黄色溶液
蓝色溶液
D. 检验试液中的CO32-:试液
白色沉淀
沉淀溶解
难度: 中等查看答案及解析
-
用如图所示装置进行下列实验,能达到实验目的的是( )

A. 瓶中盛适量浓硫酸,从A口进气来干燥NH3
B. 从B口进气,用排空气法收集SO2
C. 瓶中盛满水,从B口进气,用排水法收集NO2
D. 瓶中盛满水,A口连接导管并伸入量筒中,从B口进气用排水法测量生成NO的体积,
难度: 中等查看答案及解析
-
如图是用稀硝酸和Cu制取少量NO并验证氮氧化合物性质的装置。下列说法不正确的是( )
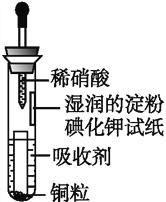
A. 吸收剂可以是NaOH溶液
B. 试管上部的气体始终为无色
C. 小试管中溶液最终呈蓝色
D. 试纸最终呈蓝色
难度: 中等查看答案及解析
-
已知:2KMnO4+16HCl═2KCl+5Cl2↑+2MnCl2+8H2O,如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.对实验现象的“解释或结论”正确的是( )
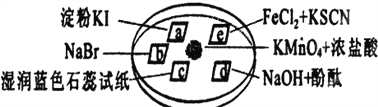
选项
实验现象
解释或结论
A
a处变蓝,b处变红棕色
氧化性:Cl2>I2 Cl2>Br2
B
c处先变红,后褪色
氯气与水生成了酸性物质
C
d处立即褪色
氯气与水生成了漂白性物质
D
e处变红色
还原性:Cl->Fe2+
A. A B. B C. C D. D
难度: 中等查看答案及解析