-
NA为阿伏加罗常数,下列有关说法正确的是( )
A.在120gNaHSO4晶体中,含阳离子数为2NA
B.足量的铜与含2molH2SO4的浓硫酸充分反应,可生成NA个SO2分子
C.500mL2mol•L-1Na2CO3溶液中,含NA个CO32-
D.1molH3O+中含有电子数为10NA难度: 中等查看答案及解析
-
1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A.Na2CO3
B.Na2O2 Na2CO3
C.NaOH Na2CO3
D.Na2O2 NaOH Na2CO3难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.过氧化钠和水反应:2+2H2O=4OH-+O2↑
B.亚硫酸氢铵和氢氧化钠的反应:NH4++OH-=NH3↑+H2O
C.碳酸氢镁溶液中加入足量的澄清石灰水:Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
D.足量的溴化亚铁和少量的氯气反应:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-难度: 中等查看答案及解析
-
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互关系,图中每条连线两端的物质均可以发生化学反应.下列推断不合理的是( )
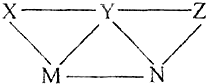
A.X一定为H2SO4
B.Y一定为K2CO3
C.Z可能是氯水
D.M、N必定各为BaCl2、FeSO4中的一种难度: 中等查看答案及解析
-
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)+Y(g)⇌2Z(g);△H<0.当改变某个条件并达到新平衡后,下列叙述正确的是( )
A.升高温度,X的体积分数减小
B.保持容器体积不变,充入一定量的惰性气体,Y的浓度不变
C.增大压强,Z的浓度不变
D.保持容器体积不变,充入一定量的Z,X的物质的量分数增大难度: 中等查看答案及解析
-
某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是( )
A.若溶液中c(A-)=c(Na+),则溶液一定呈中性
B.溶液中不可能存在:c(Na+)>c (A-)>c(OH-)>c(H+)
C.若c(OH-)>c(H+),溶液中不可能存在:c(Na+)>c(OH-)>c(A-)>c(H+)
D.若溶质为NaA、HA,则一定存在:c(A-)>c(Na+)>c(H+)>c(OH-)难度: 中等查看答案及解析
-
1L某混合溶液中,溶质X、Y的浓度都为0.1mol•L-1,向混合溶液中滴加某溶液Z至溶液呈中性,所得沉淀的物质的量如图所示,则X、Y、Z分别是( )
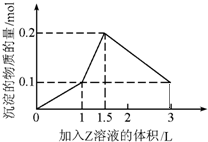
A.氯化铝、氯化铁、氢氧化钠
B.氯化铝、氯化镁、氢氧化钠
C.偏铝酸钠、氢氧化钡、硫酸
D.偏铝酸钠、氯化钡、硫酸难度: 中等查看答案及解析