-
下列变化一定会引起平衡移动的是
①反应速率的变化 ②浓度的变化 ③各组分百分含量的变化 ④平均相对分子质量的变化
⑤颜色的变化 ⑥混合气体密度的变化 ⑦转化率的变化 ⑧温度的变化
A.①②⑥⑦⑧ B.②④⑤⑥⑧ C.②④⑤⑥⑦ D.③④⑦⑧
难度: 中等查看答案及解析
-
某温度下,反应H2(g)+I2(g)
2HI(g)在密闭容器中达到平衡,缩小容器体积,增大压强,则下列说法正确的是
A.平衡正向移动 B.正反应速率增大
C.容器内I2(g)增多 D.容器内H2的质量分数增大
难度: 中等查看答案及解析
-
对于密闭容器中进行的反应N2(g)+3H2(g)
2NH3(g),达到平衡时,若温度保持不变,增加N2的浓度,则
A.正、逆反应速率同时增大 B.逆反应速率先减小
C.化学平衡逆向移动 D.化学平衡正向移动
难度: 中等查看答案及解析
-
如图为某化学反应的速率与时间的关系示意图。在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是

A.2SO2(g)+O2(g)
2SO3(g) ΔH<0
B.4NH3(g)+5O2(g)
4NO(g)+6H2O(g) ΔH<0
C.H2(g)+I2(g)
2HI(g) ΔH>0
D.2A(g)+B(g)
2C(g) ΔH>0
难度: 中等查看答案及解析
-
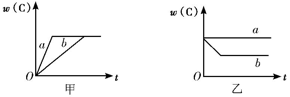
将A与B的混合气体分别置于恒压容器甲和恒容容器乙中,发生反应:2A(g) + 2B(g)
3C(g) ΔH<0。下列说法不正确的是

A.在相同条件下两容器内的反应均达到化学平衡状态,升温时甲、乙两容器中反应速率均增大
B.在相同条件下两容器内的反应均达到化学平衡状态,升温时甲、乙两容器中的平衡均向逆反应方向移动
C.在相同温度下,甲容器中加入2 mol A和2 mol B,乙容器中加入2 mol A和2 mol B,若甲容器中反应经30 s达到平衡状态,则乙容器中反应达到平衡所需要的时间也是30 s
D.在相同的温度和压强下,用甲容器分别进行如下反应。第一次加入2 mol A和2 mol B;第二次加入2 mol A、2 mol B和3 mol C;第三次加入4 mol C。分别达到化学平衡状态时,C的物质的量百分含量分别为X、Y、Z,则X、Y、Z的大小关系是X=Y=Z
难度: 中等查看答案及解析
-
X、Y混合气体在密闭容器中发生反应:aX(g)+bY(g)
cZ(g) ΔH<0;达到化学平衡后,测得X气体的浓度为0.5 mol/L;恒温条件下将密闭容器的容积扩大一倍并再次达到平衡时,测得X气体的浓度为0.3 mol/L。则下列叙述正确的是
A.平衡向右移动 B.a+b>c
C.Y的转化率提高 D.Z的体积分数增加
难度: 中等查看答案及解析
-
某温度下反应:ClF(g)+F2(g)
ClF3(g)△H<0,在密闭容器中达到平衡,下列说法中正确的是
A.温度不变,缩小体积,ClF的转化率增大
B.温度不变,增大体积,ClF3的产率提高
C.升高温度,增大体积,有利于平衡向正向移动
D.降低温度,体积不变,F2的转化率减小
难度: 中等查看答案及解析
-
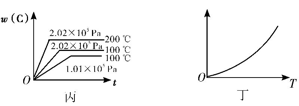
对于可逆反应N2 (g)+ 3H2 (g)
2NH3 (g)△H<0,下列研究目的和图示相符的是
研究目的
图示
A
压强对反应的影响(p2>p1)

B
温度对反应的影响

C
平衡体系增加N2对反应的影响

D
催化剂对反应的影响

难度: 中等查看答案及解析
-
对于密闭容器中的可逆反应:mX(g)+nY(s)
pZ(g) ΔH<0,达到平衡后,改变条件,下列表述不正确的是
A.增大压强,化学平衡不一定发生移动
B.通入氦气,化学平衡不一定发生移动
C.增加X或Y的物质的量,化学平衡一定发生移动
D.其他条件不变,升高温度,化学平衡一定发生移动
难度: 中等查看答案及解析
-
在温度一定的条件下,N2(g)+ 3H2(g)
2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为
,N2与NH3的浓度均为c mol·L−1。若将容器的体积压缩为原来的1/2,当达到新的平衡时,下列说法中不正确的是
A.新的平衡体系中,N2的浓度小于2c mol·L−1大于c mol·L−1
B.新的平衡体系中,NH3的浓度小于2c mol·L−1大于c mol·L−1
C.新的平衡体系中,混合体的平均摩尔质量大于
D.新的平衡体系中,气体密度是原平衡体系的2倍
难度: 中等查看答案及解析