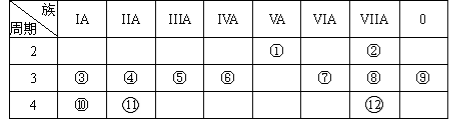
-
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列电子式中,正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列分子中所有原子都满足最外层为8个电子结构的是
A.BF3 B.CCl4 C.H2O D.PCl5
难度: 中等查看答案及解析
-
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
A.HX B.H2X C.XH4 D.XH3
难度: 中等查看答案及解析
-
下列说法中,不符合ⅦA族元素性质特征的是
A.从上到下原子半径逐渐减小 B.易形成-1价离子
C.最高价氧化物的水化物显酸性 D.从上到下氢化物的稳定性依次减弱
难度: 中等查看答案及解析
-
下列关于元素周期表和元素周期律的说法错误的是
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多
B.第二周期元素从Li到F,非金属性逐渐增强
C.因为Na比K容易失去电子,所以Na比K的还原性强
D.O与S为同主族元素,且O比S的非金属性强
难度: 中等查看答案及解析
-
下列物质中,既有离子键,又有非极性共价键的是
A.H2O B.CaCl2 C.KOH D.Na2O2
难度: 中等查看答案及解析
-
已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
难度: 中等查看答案及解析
-
下列反应既是氧化还原反应,又是吸热反应的是
A.铝片与稀H2SO4的反应 B.Ba(OH)2·8H2O与NH4+Cl的反应
C.灼热的炭与CO2的反应 D.甲烷在O2中的燃烧反应
难度: 中等查看答案及解析
-
一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是
A.浓硫酸与水 B.生石灰与水 C.熟石灰与水 D.氯化钠与水
难度: 中等查看答案及解析
-
下列各组物质中,互为同位素的是
A.
和
B.O2和O3 C.NO和NO2 D.H2O和H2O2
难度: 中等查看答案及解析
-
下列各组物质的性质比较,正确的是
A.酸性:HClO4>H3PO4>H2SO4
B.氢化物稳定性:H2S>HF>H2O
C.碱性:Al(OH)3 >Mg(OH)2>NaOH
D.氧化性:F2 > Cl2 > Br2 > I2
难度: 中等查看答案及解析
-
镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是
A.镭比钙的金属性更强 B.在化合物中呈+2价
C.镭是一种放射性元素 D.氢氧化镭呈两性
难度: 中等查看答案及解析
-
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
A.质子数:c>d B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
难度: 中等查看答案及解析
-
下列用电子式表示的形成过程正确的是( )
A.
B.
C.
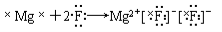
D.
难度: 中等查看答案及解析
-
如图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是( )
A.原子半径:W>Z>Y>X
B.气态氢化物的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物可能为强碱
难度: 中等查看答案及解析