-
下列变化中,属于化学变化的是( )




A.铁水铸成锅 B.折纸鹤 C. 烧制陶瓷 D. 编制中国结
难度: 简单查看答案及解析
-
发明联合制碱法,为纯碱和氮肥工业技术的发展作出了杰出贡献的科学家是( )
A.张青莲 B.侯德榜 C.门捷列夫 D.拉瓦锡
难度: 简单查看答案及解析
-
糖块放到水里会逐渐“消失”,而水却有了甜味.这一现象说明( )
A.分子的体积很小 B.分子是由原子构成的
C.分子在不断运动 D.分子本身发生了变化
难度: 简单查看答案及解析
-
下列实验操作正确的是( )
A.

点燃酒精灯
B.

往试管中加入锌粒
C.

称量氢氧化钠
D.

收集氧气
难度: 中等查看答案及解析
-
水是一种重要的自然资源.下列有关水的认识正确的是( )
A.水是人体必需的营养素之一
B.长期饮用纯净水有利身体健康
C.生活中可以通过过滤把硬水转变为软水
D.水通电分解生成氢气和氧气的体积比为2:1,说明水是由2个氢元素和1个氧元素组成的
难度: 简单查看答案及解析
-
利用能源、节约能源是我们大家共同关注的社会问题.下列属于节能图标的是( )
A.

B.

C.

D.

难度: 简单查看答案及解析
-
下列实验现象描述不正确的是( )
A.纯羊毛制品点燃后有烧焦羽毛气味产生
B.黄铜片与铜片互相刻画,黄铜片可以在铜片上画出痕迹
C.硫在空气中燃烧产生明亮的蓝紫色火焰,生成有刺激性气味的气体
D.将少量熟石灰粉末与硝酸铵固体混合、研磨,能嗅到强烈的刺激性气味
难度: 中等查看答案及解析
-
2014年世界环境日中国的主题是“向污染宣战”.下列措施可以减少污染的是( )
A.工广烟囱架高 B.提倡使用公共交通工具或步行
C.随意丢弃废旧电池 D.为了提高农作物产量,过量使用农药化肥
难度: 简单查看答案及解析
-
如图是元素周期表中某元素信息示意图,由图所获取的信息正确的是( )

A.该元素为金属元素 B.该元素的相对原子质量为35.453g
C.该元素位于元素周期表的第三周期 D.该元素在化学反应中容易失去电子
难度: 中等查看答案及解析
-
我国曾多次发生将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件.(NaNO2)中氮元素的化合价是( )
A.+2 B.+3 C.+4 D.+5
难度: 中等查看答案及解析
-
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,现将8gA和5gB2充分反应,则生成AB2的质量是( )
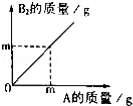
A.10g B. 13g C. 16g D. 18g
难度: 中等查看答案及解析
-
除去下列物质中的少量杂质,所选用的试剂及反应类型均正确的是
选项
物质(括号内为杂质)
试剂
反应类型
A
CO2(CO)
足量 CuO
化合反应
B
CuO(Cu)
足量 O2
置换反应
C
H2O(H2O2)
足量 MnO2
分解反应
D
Ca(OH)2(CaO)
适量稀盐酸
复分解反应
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
在常温下,将下列物质各5g分别放入50g水中,充分搅拌,现象最相似的是( )
A. CaO,NaOH B. NaCl,FeCl3 C.CaCO3,Na2CO3 D.KNO3,NH4NO3
难度: 简单查看答案及解析
-
已知元素化合价升高,该物质具有还原性.现有反应:2Na+H2O=2NaOH+H2↑,该反应中具有还原性是( )
A.Na B. H2O C. NaOH D. H2
难度: 中等查看答案及解析
-
下列各图中●和○分别表示两种不同元素的原子.有关说法正确的是( )
A.
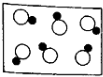
图表示混合物
B.

图表示单质
C.

图表示化合物
D.
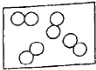
图可能是氧化物
难度: 中等查看答案及解析
-
下列物质俗称、学名、化学式一致的是( )
A.水银 汞 Hg B.纯碱 氢氧化钠 NaOH
C.生石灰 氧化钙 CaO2 D.小苏打 碳酸钠 NaHCO3
难度: 简单查看答案及解析
-
日前,一种集观赏与空气净化于一体的工艺品炭雕(如图所示,主要成分是木炭)成为了家装的新宠.炭雕之所以能用于空气净化是源于它具有( )

A. 稳定性 B. 吸附性 C. 可燃性 D. 还原性
难度: 中等查看答案及解析
-
分离下列各组混合物,其操作包括溶解、过滤、结晶三个步骤的是( )
A.氯化钾和二氧化锰 B.氯化钠和硝酸钾
C.氧化铁和氧化铝 D.硝酸铜和氢氧化钠
难度: 中等查看答案及解析
-
青少年摄入锌不足会引起食欲不振,生长迟缓,发育不良,缺锌者可在医生指导下服用葡萄糖酸锌口服液来补锌.已知葡萄糖酸锌的化学式为C12H22O14Zn.下列说法正确的是( )
A.葡萄糖酸锌口服液是纯净物
B.葡萄糖酸锌中碳、氢元素质量比为6:11
C.葡萄糖酸锌中锌元素的质量分数为14.3%
D.葡萄糖酸锌是由12个碳原子、22个氢原子、14个氧原子和1个锌原子构成的
难度: 中等查看答案及解析
-
下列各组溶液混合,能发生化学反应,并且一定能得到无色透明溶液的是( )
A.CuSO4,NaOH,NaCl B.NaCl,KCl,KNO3
C.NaOH,NaCl,HCl D.MgCl2,AgNO3,NaOH
难度: 困难查看答案及解析
-
如图是A、B、C三种物质的溶解度曲线图,请看图回答问题:

(1)20℃时,A、B、C三种物质的溶解度由小到大的顺序是 _________ ;
(2)50℃时,将30gA物质放入50g水中,充分溶解,所得溶液为 _________ (填“饱和”或“不饱和”)溶液,此时溶液中溶质质量分数为 _________ ;(精确到0.1%)
(3)使一定量接近饱和的C物质溶液变成饱和溶液,采用的一种方法是 _________ .
难度: 中等查看答案及解析