-
进行过滤操作应选用的一组仪器是( )
A. 滤纸、烧杯、试管、漏斗、玻璃棒
B. 烧杯、酒精灯、试管、漏斗
C. 漏斗、玻璃棒、烧杯、铁架台、滤纸
D. 玻璃棒、滤纸、蒸馏烧瓶、漏斗、铁架台
难度: 简单查看答案及解析
-
某溶液中含有较大量的Cl-、CO32-、OH-3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是 ( )
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液④滴加Ba(NO3)2溶液
A. ①②④②③ B. ④②①②③
C. ①②③②④ D. ④②③②①
难度: 中等查看答案及解析
-
下图分别表示四种操作,其中有两个错误的是( )
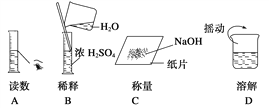
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ⑥泥三角 ⑦坩埚 ⑧铁三脚架
A. ③⑥⑦⑧ B. ②③⑤⑧ C. ①③④⑤ D. ②③⑤⑥
难度: 简单查看答案及解析
-
某学生用托盘天平称量食盐,将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5 g(1 g以下用游码)。该学生所称量的食盐的实际质量是( )
A. 15.5 g B. 15.0 g C. 14.5 g D. 16.0 g
难度: 简单查看答案及解析
-
某氯原子的质量是ag,12C原子的质量是bg,用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
①该氯原子的相对原子质量为
②mg该氯原子的物质的量为
mol
③该氯原子的摩尔质量是aNAg ④ag该氯原子所含的电子数为17mol
A. ①③ B. ②④ C. ①② D. ②③
难度: 简单查看答案及解析
-
同质量的下列气体中,所含原子数最少的是 ( )
A.CH4 B.CO2 C.H2S D.N2
难度: 中等查看答案及解析
-
下列说法正确的是
A.在常温常压下,11.2LN2所含有的分子数为0.5NA
B.在标准状况下, 22.4 L CO和N2的混合物的物质的量为1mol
C.在标准状况下, 18g H2O的体积为22.4 L
D.1mol SO2的体积为22.4 L
难度: 中等查看答案及解析
-
4 ℃时,若20滴水恰好为1 mL,那么1滴水中所含的水分子数约为(NA表示阿伏加德罗常数的值)( )
A. 20NA B. NA/360
C. 9NA/10 D. 360/NA
难度: 中等查看答案及解析
-
下列溶液中物质的量浓度为1mol/L的是
A.将40gNaOH 溶解在1L水中
B.将22.4LHCl气体溶于水配成1 L溶液
C.将1L 10 mol/L的浓盐酸加入9 L水中
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
难度: 中等查看答案及解析
-
将5 mol/L的盐酸10 mL稀释到200 mL,取出5 mL,这5 mL溶液的物质的量浓度为
A. 0.5 mol/L B. 0.25 mol/L C. 0.1 mol/L D. 1 mol/L
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA
B. 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
C. 标准状况下,11.2 L CCl4含有分子数为0.5 NA
D. 1 mol·L-1的Na2CO3溶液中含有2NA个Na+
难度: 困难查看答案及解析
-
等温等压下,有质子数相等的CO、N2、C2H2三种气体,下列叙述中正确的是( )
A. 密度之比为14∶14∶13 B. 体积之比为13∶13∶14
C. 质量之比为1∶1∶1 D. 原子数之比为1∶1∶1
难度: 困难查看答案及解析