-
约占空气体积五分之一的气体是
A. 氧气 B. 氮气 C. 二氧化碳 D. 水蒸气
难度: 简单查看答案及解析
-
属于化学变化的是
A. 海水晒盐 B. 河水结冰 C. 石灰石制生石灰 D. 分离空气制氧气
难度: 简单查看答案及解析
-
核电站用硼酸(H3BO3)阻断核辐射,硼酸中硼元素(B)的化合价是
A. +1 B. +2 C. +3 D. +4
难度: 简单查看答案及解析
-
能减少氧气在水中溶解度的方法是
A. 升高温度 B. 减少氧气的体积 C. 减少水的质量 D. 增大压强
难度: 简单查看答案及解析
-
不是同素异形体的一组物质是
A. 金刚石和石墨 B. 氧气和臭氧 C. 红磷和白磷 D. 氧化铁和氧化亚铁
难度: 简单查看答案及解析
-
物质在氧气中燃烧,产生明亮蓝紫色火焰的是
A. 铁丝 B. 木炭 C. 硫粉 D. 镁带
难度: 简单查看答案及解析
-
下列物质在水中,不能形成溶液的是
A. 食盐 B. 氢氧化钙 C. 泥土 D. 二氧化碳
难度: 简单查看答案及解析
-
含游离态氧元素的物质是
A. 过氧化氢 B. 空气 C. 二氧化碳 D. 水
难度: 简单查看答案及解析
-
有关碳酸钾的说法错误的是
A. 是草木灰的主要成分 B. 可用做钾肥
C. 是一种正盐 D. 焰色反应呈黄色
难度: 简单查看答案及解析
-
不属于有机物的是
A. 碳酸 B. 酒精 C. 淀粉 D. 甲烷
难度: 简单查看答案及解析
-
能用质量守恒思想解释,并推论正确的是
A. 50mL36%的盐酸用50mL水稀释,推出稀盐酸的溶质质量分数为18%
B. 某物质燃烧生成二氧化碳和水,推出该物质一定含有碳、氢元素
C. 10克食盐溶于70克水中能形成80克食盐水
D. 铁丝在氧气中燃烧,推出反应前后固体质量不变
难度: 简单查看答案及解析
-
粗盐提纯中,描述正确的是
A. 溶解、过滤、蒸发都用到玻璃棒,但作用不同
B. 蒸发时,开始析出晶体后用玻璃棒搅拌
C. 蒸发时,待水分完全蒸干后停止加热
D. 过滤时,用玻璃棒搅拌加快过滤速度
难度: 简单查看答案及解析
-
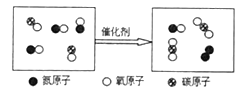
电解水实验的说法错误的是
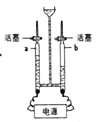
A. 水电解成H2和O2的分子数比为2:1,根据原子守恒推出水分子中H、O原子数比为2:1
B. 反应一段时间后,a、b玻璃管中产生的气体质量比约为8:1
C. 负极产生的气体使带火星木条复燃,正极产生的气体能被点燃
D. 由电解水实验得出结论:水是由氢、氧两种元素组成的
难度: 中等查看答案及解析
-
配制一定质量分数的稀硫酸,用到的一组仪器是
A. 天平、量筒、烧杯、酒精灯 B. 烧杯、量筒、玻璃棒、胶头滴管
C. 天平、药匙、量筒、烧杯 D. 量筒、烧杯、试管、玻璃棒
难度: 简单查看答案及解析
-
物质的用途错误的是
A. 稀硫酸用于除去铁钉表面的铁锈 B. 二氧化碳用于呼吸作用
C. 活性炭用于吸附水中悬浮杂质 D. 稀有气体用于制霓虹灯
难度: 简单查看答案及解析
-
有关规律的描述中正确的是
A. “碳”是一个大家族,所有物质都含有碳元素
B. 所有盐中都一定含有金属元素
C. 金属与酸发生置换反应后,溶液的质量都会增加
D. 能使石蕊试液变蓝的溶液一定是碱溶液
难度: 中等查看答案及解析
-
关于分子、原子的叙述正确的是
A. 原子是不能再分的最小微粒
B. 分子能构成物质,原子不能构成物质
C. 分子和原子在不停的运动
D. 分子之间有间隙,原子之间没有间隙
难度: 简单查看答案及解析
-
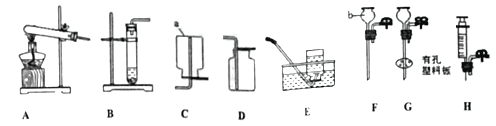
水在化学实验中的作用有许多,下列实验中对水的作用,解释错误的是
A
B
C
D
实验
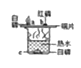
硫的燃烧
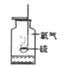
检查气密性
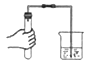
准备过滤器
作用
隔绝空气和加热
防止炸裂瓶底
形成密闭系统,用于观察检查装置是否漏气
用胶头滴管滴少量水,让滤纸紧贴漏斗内壁
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
把铁粉加入Ag(NO3)2、Cu(NO3)2、Zn(NO3)2的混合溶液中,充分反应后,过滤。正确的分析是
A. 如滤液中含有Cu(NO3)2、Fe(NO3)2、Zn(NO3)2,则滤出的固体中只含有Ag
B. 如滤液中含有Fe(NO3)2、Zn(NO3)2,没有Cu(NO3)2,则滤出固体中有Cu、Ag,可能有Fe
C. 如滤出固体中有Ag、Cu,则滤液中有Zn(NO3)2、Fe(NO3)2,没有AgNO3、Cu(NO3)2
D. 如滤出固体中有Ag、Cu、Fe,滤液中一定含有Zn(NO3)2、Fe(NO3)2,可能含Cu(NO3)2
难度: 困难查看答案及解析
-
下列各组转化关系中的反应为初中化学常见的反应,其中的“→”表示某种物质可一步反应生成另一种物质。甲、乙、丙三种物质不符合对应“转化关系”的是
选项
A
B
C
D
转化关系
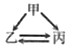
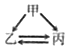
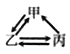
物质
甲
H2O2
C
CaCO3
CuCl2
乙
O2
CO
CO2
Cu
丙
H2O
CO2
Na2CO3
CuO
A. A B. B C. C D. D
难度: 中等查看答案及解析