-
下列对物质分类的归纳中,错误的是( )
A.蔗糖、酒精、甲烷等这类含碳化合物属于有机物
B.由金属离子和酸根离子组成的化合物称为盐
C.能电离出氢离子的化合物一定为酸
D.与酸反应,只生成盐和水的氧化物,通常称为碱性氧化物难度: 中等查看答案及解析
-
有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(即碳酸钙粒子直径是纳米级),这将引起建筑材料的性能发生巨变.下列关于纳米碳酸钙的推测可能正确的是( )
A.纳米碳酸钙是与胶体相似的分散系
B.纳米碳酸钙分散到水中会产生丁达尔效应
C.纳米碳酸钙化学性质已与原来碳酸钙完全不同
D.纳米碳酸钙的粒子不能透过滤纸难度: 中等查看答案及解析
-
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于
区域3的是( )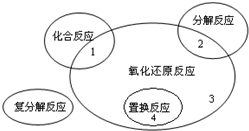
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.CH4+2O2═CO2+2H2O难度: 中等查看答案及解析
-
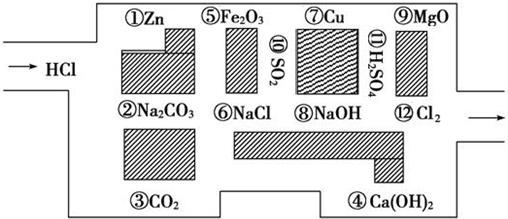
下列物质间的转化能一步实现的是( )
A.Na2CO3→NaOH
B.CaCO3→Ca(OH)2
C.NaNO3→NaCl
D.FeSO4→CuSO4难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol NH4+ 所含质子数为10NA
B.10克氖气所含原子数约为NA
C.标准状况下,22.4 L H2O所含的分子数为NA
D.常温常压下,32 g O2和O3的混合气体所含原子数为2NA难度: 中等查看答案及解析
-
下列化学用语书写正确的是( )
A.中子数为8的碳原子:C
B.纯碱的化学式:NaHCO3
C.硫酸的电离方程式:H2SO4=H2++SO42-
D.氯离子的结构示意图为: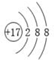
难度: 中等查看答案及解析
-
实验室里需用480mL 0.1mol/L的硫酸铜溶液,现选取500mL容量瓶进行配制,以下设想合理的是( )
A.称取7.68g CuSO4,配成480mL的溶液
B.称取12.0g CuSO4•5H2O,配成480mL的溶液
C.称取8.0g CuSO4,加入500mL水
D.称取12.5g CuSO4•5H2O,配成500mL溶液难度: 中等查看答案及解析
-
物质发生化学变化时,下列量在反应前后肯定不发生变化的是( )
①电子总数 ②原子总数 ③分子总数 ④物质种类 ⑤物质的总质量 ⑥物质的总能量.
A.①②⑤
B.①②③⑤
C.②⑤⑥
D.①④⑤⑥难度: 中等查看答案及解析
-
下列溶液中Cl-浓度与50mL 1mol•L-1 AlCl3溶液中Cl-浓度相等的是( )
A.150mL 1mol•L-1的NaCl溶液
B.75mL 2mol•L-1 NH4Cl溶液
C.25mL 1.5mol•L-1的MgCl2溶液
D.75mL 3mol•L-1的KClO3溶液难度: 中等查看答案及解析
-
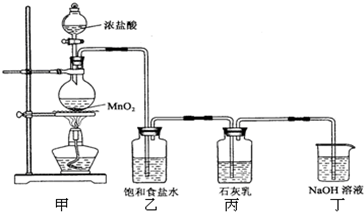
下列常用干燥剂中:①无水CaCl2 ②碱石灰 ③浓H2SO4 ④P2O5,可以用来干燥Cl2的是( )
A.①②③
B.①②④
C.①③④
D.②③④难度: 中等查看答案及解析
-
下列混合物能用溶解、过滤、蒸发三步操作分离的是( )
A.水和酒精的混合物
B.氯化钠固体和硝酸钾固体的混合物
C.氯化钾固体和氯化银固体的混合物
D.硫酸钡固体和碳酸钡固体的混合物难度: 中等查看答案及解析
-
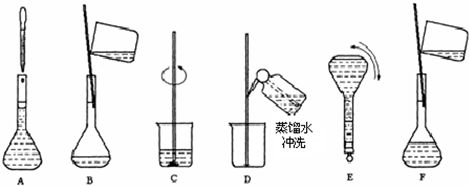
下列实验操作中错误的是( )
A.进行蒸发操作时,蒸发皿中出现大量固体时,即可停止加热
B.进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大难度: 中等查看答案及解析
-
在某密闭容器中通入a mol NO和b mol O2,发生反应:2NO+O2=2NO2,反应后容器内氮原子和氧原子之比为( )
A.a:b
B.a:(a+2b)
C.a:2b
D.a:2(a+b)难度: 中等查看答案及解析
-
将下列各组物质区别开来的实验方案(见括号内的方法)不合理的是( )
A.Na2CO3和NaHCO3(采用加氯化钙溶液观察有无沉淀的方法)
B.(NH4)2SO4与NH4Cl(采用加氢氧化钠溶液并加热闻其气味的方法)
C.NaCl与KCl(采用灼烧时观察焰色的方法)
D.K2CO3与KNO3(采用加稀盐酸观察有无气泡产生的方法)难度: 中等查看答案及解析
-
实验室用下列两种方法制氯气:①用含HCl 146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应.所得的氯气( )
A.①比②多
B.②比①多
C.一样多
D.无法比较难度: 中等查看答案及解析
-
已知元素R有某种同位素的氯化物RClX,该氯化物中RX+的核外电子数为Z,核内中子数为Y,该同位素可表示为( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
质量相同的两种气体A、B,在同温、同压下,A的分子数比B多.下列说法正确的( )
A.A占的体积比B小
B.A的摩尔质量比B大
C.A的密度比B小
D.A的物质的量比B小难度: 中等查看答案及解析
-
如图是某溶液在稀释过程中,溶质的物质的量浓度随溶液体积的变化曲线图,根据图中数据分析可得出a值等于( )
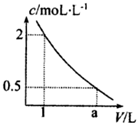
A.2
B.3
C.4
D.5难度: 中等查看答案及解析
-
有一真空储气瓶质量为400g,在相同条件下,装满O2时质量为404克,装满另一种气体X时质量为405.5克,则X的相对分子质量为( )
A.44
B.64
C.71
D.48难度: 中等查看答案及解析
-
下表中列出了一定压强和温度下每立方厘米活性炭所能吸附的常见气体的体积,分析表中数据与气体的组成、性质的关系,你认为下列结论正确的是( )
气体性质 H2 CO2 O2 CO Cl2 气体的沸点/℃ -252 -78 -183 -196 -34 被吸附体积/mL 4.5 97 35 11 494
A.每个气体分子所含原子个数越多,越容易被吸附
B.沸点越低的气体,越易被吸附
C.气体是化合物时,易被吸附
D.气体的相对分子质量越大,越易被吸附难度: 中等查看答案及解析