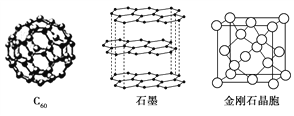
-
干冰气化时,下列所述内容发生变化的是( )
A. 分子内共价键 B. 分子间作用力 C. 分子的性质 D. 分子间的氢键
难度: 简单查看答案及解析
-
根据下列性质判断,属于原子晶体的物质是
A.熔点2 700 ℃,导电性好,延展性强
B.无色晶体,熔点3 500 ℃,不导电,质硬,难溶于水和有机溶剂
C.无色晶体,能溶于水,质硬而脆,熔点800 ℃,熔化时能导电
D.熔点-56.6 ℃,微溶于水,硬度小,固态或液态时不导电
难度: 中等查看答案及解析
-
碘的熔、沸点低,其原因是( )
A. 碘的非金属性较弱 B. I—I键的键能较小
C. 碘晶体属于分子晶体 D. I—I共价键的键长较长
难度: 简单查看答案及解析
-
我国的激光技术在世界上处于领先地位,据报道,有科学家用激光将置于铁室中石墨靶上的碳原子炸松,与此同时再用射频电火花喷射氮气,此时碳、氮原子结合成碳氮化合物薄膜。据称,这种化合物可能比金刚石更坚硬。其原因可能是( )
A. 碳、氮原子构成平面结构的晶体 B. 碳氮键比金刚石中的碳碳键更短
C. 氮原子电子数比碳原子电子数多 D. 碳、氮的单质的化学性质均不活泼
难度: 简单查看答案及解析
-
二氧化硅晶体是空间立体网状结构,如图所示。下列关于二氧化硅晶体的说法中不正确的是( )
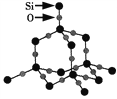
A. 1 mol SiO2晶体中含2 mol Si—O键 B. 晶体中Si、O原子个数比为1:2
C. 晶体中Si、O原子最外电子层都满足8电子稳定结构 D. 晶体中最小环上的原子数为12
难度: 中等查看答案及解析
-
下列性质适合于分子晶体的是( )
①熔点1 070℃,易溶于水,水溶液导电
②熔点10.31℃,液态不导电,水溶液导电
③能溶于CS2,熔点112.8℃,沸点444.6℃
④熔点97.81℃,质软、导电,密度为0.97 g·cm-3
A. ①② B. ①③ C. ②③ D. ②④
难度: 简单查看答案及解析
-
美国《科学》杂志曾报道:在40 GPa的高压下,用激光加热到1800 K,人们成功制得了原子晶体CO2,下列对该物质的推断一定不正确的是( )
A. 该原子晶体中含有极性键 B. 该原子晶体易气化,可用作制冷材料
C. 该原子晶体有很高的熔点 D. 该原子晶体硬度大,可用作耐磨材料
难度: 中等查看答案及解析
-
下列各组物质发生状态变化时,所克服的微粒间的相互作用,属于同种类型的是( )
A. 金刚石和硫的熔化 B. 食盐和石蜡的熔化
C. 碘和干冰的升华 D. 二氧化硅和氧化钠的熔化
难度: 简单查看答案及解析
-
支持固态氨是分子晶体的事实为( )
A. 氮原子不能形成阳离子 B. 铵离子不能单独存在
C. 常温下氨是气态物质 D. 氨极易溶于水
难度: 简单查看答案及解析
-
目前,科学界拟合成一种“二重构造”的球形分子,即把“足球形”的C60熔进“足球形”的Si60分子中,外面的硅原子与里面的碳原子以共价键结合。下列关于这种分子的说法中不正确的是( )
A. 是一种新型化合物 B. 晶体属于分子晶体
C. 是两种单质组成的混合物 D. 相对分子质量为2400
难度: 中等查看答案及解析
-
目前,世界上已合成了几百种有机超导体,TCNQ就是其中之一。TCNQ的分子结构如下图所示。下列关于TCNQ的说法中错误的是( )
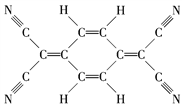
A. 分子中所有的氮原子在同一平面内 B. 属于原子晶体
C. 化学式为C12H4N4 D. 该物质难溶于水
难度: 简单查看答案及解析
-
关于SiO2晶体的叙述中,正确的是( )
A. 通常状况下,60 g SiO2晶体中含有的分子数为NA(NA表示阿伏加德罗常数)
B. 60 g SiO2晶体中,含有2NA个Si—O键
C. 晶体中与同一硅原子相连的4个氧原子处于同一四面体的4个顶点
D. SiO2晶体中含有1个硅原子,2个氧原子
难度: 中等查看答案及解析
-
已知C3N4晶体具有比金刚石还大的硬度,且构成该晶体的微粒间只以单键结合。下列关于C3N4晶体的说法错误的是( )
A. 该晶体属于原子晶体,其化学键比金刚石中的碳碳键更牢固
B. 该晶体中每个碳原子连接4个氮原子,每个氮原子连接3个碳原子
C. 该晶体中碳原子和氮原子的最外层都满足8电子结构
D. 该晶体与金刚石相似,都是原子间以非极性键形成空间网状结构
难度: 中等查看答案及解析