-
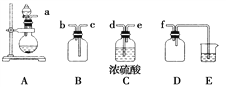
化学与人类生产、生活密切相关,下列说法正确的是
A. 大量CO2排放可导致酸雨的形成
B. 焚烧废旧塑料以防止“白色污染”
C. 绿色化学的核心是利用化学原理对环境污染进行治理
D. 硅酸多孔、吸水能力强,常用作袋装食品的干燥
难度: 中等查看答案及解析
-
唐朝诗人刘禹锡的《浪淘沙》“美人首饰侯王印,尽是沙中浪底来”从中可以得出古人从沙子中得到黄金的方法为
A. 热还原法 B. 热分解法 C. 重力沉降法 D. 电解法
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 常温常压下,16gO2和O3混合气体中含有氧原子数为NA
B. 标准况状下,44.8L氟化氢含有的分子数为2NA
C. 0.1molL-1氯化铝溶液中含有Al3+数为0.1 NA
D. 标准状况下,22.4LO2作氧化剂时转移电子数定为4 NA
难度: 中等查看答案及解析
-
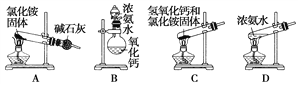
实验是化学研究的基础,下图装置或操作正确的是
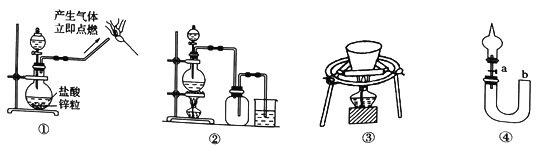
A. 用①制备氢气并检验氢气的可燃性
B. 用装置②制备SO2
C. 用装置③陶瓷坩埚高温煅烧CaCO3固体
D. 关闭活塞a,从b处加水,以检查装置④的气密性
难度: 中等查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A. 用KIO3氧化酸性溶液中的KI:5I—+IO3—+3H2O==I2+6OH—
B. 向NH4HCO3溶液中加过量Ba(OH)2溶液并加热:NH4++OH—
NH3↑+H2O
C. 在海带灰的浸出液(含有I—)中滴加H2O2得到I2:2I—+H2O2+2H+==I2+2H2O
D. 用浓硝酸洗涤试管内壁的银镜Ag+2H++NO3—==Ag++NO↑+H2O
难度: 中等查看答案及解析
-
对已达化学平衡的下列反应:2X(g)+Y(g)
2Z(g)△H>0;降低温度的同时减小压强,对反应产生的影响是
A. 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B. 逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C. 正、逆反应速率都减小,平衡向逆反应方向移动
D. 正、逆反应速率都减小,平衡向正反应方向移动
难度: 中等查看答案及解析
-
海洋约占地球表面积的71%,对其进行开发利用的部分流程如右图所示。下列说法不正确的是
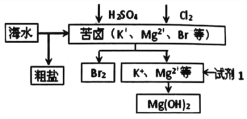
A. 可用Na2CO3溶液除去粗盐中的Ca2+
B. 从成本考虑,试剂1选用NaOH溶液
C. 从苦卤中提取Br2的反应的离子方程式为2Br—+C12===2C1—+Br2
D. 工业上,电解熔融MgCI2冶炼金属镁
难度: 中等查看答案及解析
-
某同学选择恰当的试剂和方法除去下列物质中少量杂质(括号内为杂质),下列各项中不正确的是
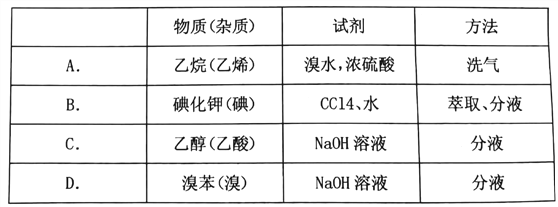
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
柠檬烯是一种食用香料,其结构简式如图
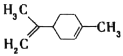 ,有关柠檬烯的分析不正确的是
,有关柠檬烯的分析不正确的是A. 它的一氯代物有8种
B. 一定条件下,它分别可以发生加成、取代、氧化、水解反应
C. 它所含的碳原子不在同一平面
D. 1mol该有机物最多可以跟2molH2加成
难度: 中等查看答案及解析
-
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是
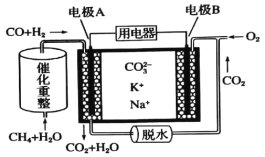
A. 电池工作时,CO32—向电极B移动
B. 电极A上H2参与的电极反应为H2+2OH—-2e—==2H2O
C. 反应CH4+H2O
3H2+CO,每消耗1 mol CH4参加反应共转移6mol电子
D. 电极B上发生的电极反应为O2+4e—+2H2O==4OH—
难度: 中等查看答案及解析
-
已知:①4NH3(g)+5O2(g)
4NO(g)+6H2O(g) ΔH1=-905.5kJ·mo1—1
②N2(g)+O2(g)
2NO(g) △H2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下
③NH3(g)+4NO(g)+O2(g)
4N2(g)+6H2Og) ΔH3=—1625.5 kJ·mo1—1
下列说法不正确的是
A. 反应③一定能自发进行
B. 反应②生成物总能量高于反应物总能量
C. 反应①使用催化剂,反应速率加快,△H1减小
D. 反应③达到平衡后改变条件,v(正)、v(逆)的变化如图所示,则该条件可能是升高温度
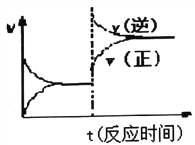
难度: 中等查看答案及解析
-
W、R、X、Y、Z是原子序数依次增大的短周期主族元素。Y原子半径在短周期主族元素中最大。W与Y同主族,X与Z同主族。R原子最外层电子数比内层电子数多1,W、R原子的电子数总和与X、Z原子的电子数总和之比为1:4。下列说法正确的是
A. 原子半径:r(X)>r(R)>r(W) B. X与Y形成的化合物只有离子键
C. X的简单气态氢化物的沸点比Z的低 D. X、Y、Z三种元素组成的盐至少有3种
难度: 中等查看答案及解析
-
常温下,不考虑混合后溶液体积的变化,下列说法正确的是
A. 0.1mol·L—1CH3COOH溶液加水稀释后,溶液中c(CH3COO—)/c(CH3COOH)的值减少
B. pH=3的CH3COOH溶液和pH=13的NaOH溶液等体积混合后恰好完全反应,则原CH3COOH溶液中 CH3COOH的电离度为1%
C. a mol·L—1H2C2O4溶液与 a mol·L—1的NaOH溶液等体积混合后,c(C2O42—)>c(HC2O4—)>c(H2C2O4)>C(OH—)
D. 0.1 mol·L—1的下列溶液中:①NH4A1(SO4)2溶液②NH4Cl溶液、③CH3COONH4溶液,c(NH4+)的大小顺序为①>③>②
难度: 中等查看答案及解析
-
下列图示与对应的叙述相符的是
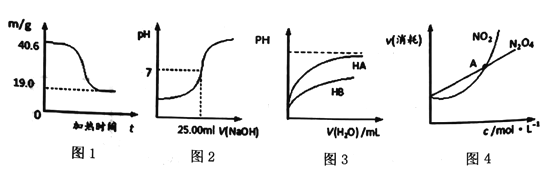
A. 图1表示0.2mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化
B. 图2表示用0.1000mo1· L—1NaOH溶液滴定25.00mLCH3COOH的滴定曲线,则c(CH3COOH)=0.100 mo1· L—1
C. 图3表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则常温下,NaA溶液的pH小于同浓度的NaB溶液的pH
D. 图4表示恒温恒容条件下,2NO2(g)
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
难度: 中等查看答案及解析