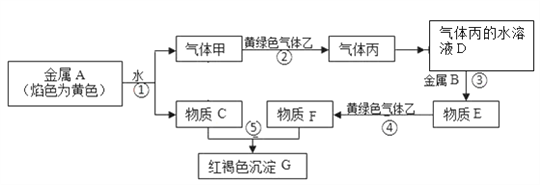
-
下列关于胶体的叙述正确的是( )
A. 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
B. 利用半透膜可除去淀粉溶液中的少量NaCl
C. Fe(OH)3胶体粒子在电场的作用下将向阴极运动,说明Fe(OH)3胶体带正电
D. 将饱和FeCl3溶液滴入沸水中,至出现红褐色的沉淀,即得Fe(OH)3胶体
难度: 简单查看答案及解析
-
下列各组中的两种物质作用时,反应条件(温度、反应物用量、反应物浓度等)改变,不会引起产物改变的是( )
A. Na2O2和CO2 B. NaOH和CO2
C. Na和O2 D. Cu和HNO3
难度: 简单查看答案及解析
-
化学与生产、生活密切相关。下列叙述正确的是 ( )
A. 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同
B. 氮的固定只有在高温、高压、催化剂的条件下才能实现
C. 喝补铁剂时,加服维生素C效果更好,原因是维生素C具有还原性
D. “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关
难度: 简单查看答案及解析
-
下列有关物质分类正确的是( )
①混合物:盐酸、氯水、氨水、冰和水混合
②化合物:CaCl2、烧碱、纯碱、O3
③电解质:H2SO4、CuSO4·5H2O、无水醋酸、硫酸钡
④同素异形体:C60、C70、金刚石、石墨
A. ①③ B. ②④ C. ②③ D. ③④
难度: 简单查看答案及解析
-
下列关于氯及其化合物的说法中错误的是( )
A. 新制的氯水应放在棕色的试剂瓶中
B. 新制氯水可使石蕊试液先变红后褪色
C. 氯气在参与的化学反应中只能作为氧化剂
D. 漂白粉可由Cl2 通入消石灰中制备,其有效成分是Ca(ClO)2
难度: 简单查看答案及解析
-
一定能在下列溶液中大量共存的离子组是( )
A. 碱性溶液:Na+、Ca2+、SO42-、CO32-
B. 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN-
C. HNO3溶液:H+、Fe2+、SO42-、Cl-
D. 含有大量H+的溶液:Na+、NH4+、SO42-、Cl-
难度: 简单查看答案及解析
-
现有①MgSO4 ②Ba(NO3)2 ③NaOH ④CuCl2四种溶液,不加其他试剂就可鉴别出来,鉴别的先后顺序是( )
A. ④③①② B. ③④①② C. ②①③④ D. ③④②①
难度: 中等查看答案及解析
-
下列对某溶液所含离子检验的叙述正确的是( )
A. 滴入BaCl2溶液和稀硝酸,产生白色沉淀,则原溶液一定含有SO42﹣
B. 滴入盐酸酸化的硝酸银溶液,产生白色沉淀,则原溶液一定含有Cl﹣
C. 滴入KSCN溶液无明显现象,再通入少量Cl2后呈红色,则原溶液一定含有Fe2+
D. 滴入NaOH溶液并加热,产生能使湿润的蓝色的石蕊试纸变红的气体,则原溶液一定含有NH4+
难度: 中等查看答案及解析
-
下表中对离子方程式的评价不合理的是( )
选项
化学反应及其离子方程式
评 价
A
向碳酸钙上滴加稀盐酸:2H++CO32﹣=CO2↑+H2O
错误,碳酸钙难溶于水,不应该写成CO32﹣
B
向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42﹣=BaSO4↓
正确
C
铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
错误,H+的氧化性较弱,只能将铁单质氧化为Fe2+
D
氯气与水反应:Cl2+2H2O=2H++Cl-+ClO-
错误,反应生成的次氯酸是弱电解质,应写成HClO
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某国外化学教材中有一张关于氧化还原反应的插图:由图可知,
 在该反应中是
在该反应中是
A. 氧化剂 B. 还原剂 C. 氧化产物 D. 还原产物
难度: 简单查看答案及解析
-
下图所示的实验操作,不能达到相应目的的是( )

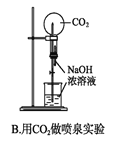


A. A B. B C. C D. D
难度: 中等查看答案及解析
-
实验室制取少量N2,常利用的反应是NaNO2+NH4Cl
NaCl+N2↑+2H2O,关于该反应的说法正确的是( )
A. NaNO2是还原剂 B. 生成1 mol N2时转移的电子数为6 mol
C. NH4Cl中的氮元素被还原 D. N2既是氧化产物又是还原产物
难度: 简单查看答案及解析
-
某溶液中含四种离子,己知其中三种离子Na+、Mg2+、NO3-的物质的量浓度分别为0.2mol·L-1,0.l mol·L-1,0.l mol·L-1,则溶液中另一离子及其物质的量浓度可能是( )
A. SO42- 0.l mol·L-1 B. Al3+ 0.2 mol·L-1
C. Cl- 0.3 mol·L-1 D. K+ 0.4mol·L-1
难度: 中等查看答案及解析
-
将0.84 g NaHCO3和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )


A. A B. B C. C D. D
难度: 中等查看答案及解析
-
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒,其中N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
A. 该反应的还原剂是Cl-
B. 反应后溶液的酸性明显增强
C. 消耗1mol还原剂,转移6mol电子
D. 氧化剂与还原剂的物质的量之比为2∶3
难度: 中等查看答案及解析