-
赏心悦目的雕花玻璃是用下列物质中的一种对玻璃进行刻蚀而制成的.这种物质是( )
A.盐酸
B.氢氟酸
C.烧碱
D.纯碱难度: 中等查看答案及解析
-
下列溶液中能够区别SO2和CO2气体的是①澄清石灰水 ②H2S溶液 ③KMnO4酸性溶液 ④氯水 ⑤品红溶液( )
A.①②③
B.②③④
C.除①以外
D.全部难度: 中等查看答案及解析
-
下列实验现象的描述错误的是( )
A.钠在空气中燃烧,发出黄色的火焰,生成淡黄色固体
B.红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒
C.点燃的硫在氧气中剧烈燃烧,发出蓝紫色火焰
D.氢气在氯气中燃烧生成白色烟雾难度: 中等查看答案及解析
-
下列叙述正确的是( )
①氧化铝是一种比较好的耐火材料,可用来制造耐火坩埚
②氧化铁常用作红色油漆和涂料
③硅酸钠是制备硅胶和木材防火剂的原料
④用纯碱、石灰石、石英为原料可制普通玻璃
⑤石灰石、高岭石、石英和水晶的主要成份都是SiO2.
A.①③④⑤
B.②③④⑤
C.①②④⑤
D.①②③④难度: 中等查看答案及解析
-
把少量NO2气体通入过量小苏打溶液中,再使逸出的气体通过装有足量的过氧化钠颗粒的干燥管,最后收集到的气体是( )
A.O2
B.NO2
C.NO2和O2
D.NO2和NO难度: 中等查看答案及解析
-
在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,可使铜粉溶解的是( )
A.②④
B.①②
C.②③④
D.①③④难度: 中等查看答案及解析
-
在抗震救灾中要用大量漂白粉和漂白液杀菌消毒.下列说法中正确的是( )
A.漂白粉是纯净物,漂白液是混合物
B.漂白粉的有效成分是Ca(ClO)2
C.工业上将氯气通入澄清石灰水制取漂白粉
D.漂白液的有效成分是Na2O2难度: 中等查看答案及解析
-
氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1molN2有6mol电子转移难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A.1molCl2与足量Fe反应,转移的电子数为3NA
B.1.5molNO2与足量H2O反应,转移的电子数为NA
C.常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA
D.NA个O2和NA个H2的质量比为16:1难度: 中等查看答案及解析
-
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因可能是( )
A.容量瓶中原来含有少量蒸馏水
B.烧杯中溶解NaOH后,未经冷却,立即转移至容量瓶并洗涤烧杯,定容
C.溶解NaOH的烧杯没有洗涤
D.向容量瓶中加水定容时眼睛一直仰视刻度线难度: 中等查看答案及解析
-
向BaCl2溶液中通入SO2至饱和,此过程无明显实验现象.再向溶液中加入一种物质,溶液变浑浊.加入的这种物质不可能是( )
A.FeCl3溶液
B.AgNO3溶液
C.稀氨水
D.NH4Cl溶液难度: 中等查看答案及解析
-
双球洗气管是一种多用途仪器,常用于除杂质、气体干燥、气体吸收等实验操作.右图是一个以双球洗气管为尾气处理装置,用吸收剂X吸收气体Y的情形,其中符合事实的组合是( )
A B C D 吸收气体Y Cl2 HCl SO2 NO 吸收剂X 饱和NaCl溶液 水 浓硫酸 NaOH溶液 
A.A、
B.B、
C.C、
D.D、难度: 中等查看答案及解析
-
下列离子方程式表示错误的是( )
A.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:
HCO3-+Ba2++OH-═BaCO3↓+H2O
B.Fe2O3溶于过量氢碘酸溶液中:
Fe2O3+6H++2I-═2Fe2++I2+3H2O
C.铜片加入稀硝酸中:
3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O
D.三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体:
Fe3++3H2O=Fe(OH)3↓+3H+难度: 中等查看答案及解析
-
进行化学实验、观察实验现象,通过分析、推理得出正确的结论是化学学习的方法之一.下列对有关实验事实的解释正确的是( )
A.将N2和过量的O2在高温或放电的条件下反应得到红棕色的气体,说明NO为红棕色气体
B.用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中含Na+
C.在AgNO3的溶液中加入锌粉,能置换出银,说明Ag+的还原性比Zn2+强
D.浓硫酸放入蔗糖中,能使蔗糖碳化,说明浓硫酸具有吸水性难度: 中等查看答案及解析
-
图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是 ( )

A.该硫酸的物质的量浓度为9.2mol•L-1
B.1molZn与足量的该硫酸反应产生2gH2
C.配制200mL4.6mol•L-1的稀硫酸需取该硫酸50mL
D.该硫酸与等体积的水混合后所得溶液的物质的量浓度等于9.2mol•L-1难度: 中等查看答案及解析
-
对某无色溶液中所含离子进行鉴别,根据实验事实所得出的相应结论正确的是( )
实 验 事 实 结论 A 加入AgNO3溶液产生白色沉淀,加稀盐酸沉淀不消失 一定有Cl¯存在 B 加入Ba(NO3)2溶液生成白色沉淀,加稀盐酸沉淀不消失 一定有SO42-存在 C 通入Cl2后溶液变为黄色,加入淀粉溶液后溶液变蓝 一定有I¯存在 D 加入紫色石蕊试液,溶液变红色 一定有OH¯存在
A.A、
B.B、
C.C、
D.D、难度: 中等查看答案及解析
-
右图是一套检验气体性质的实验装置,向装置中缓缓地通入气体X,若关闭活塞K,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红溶液褪色.据此判断气体X和洗气瓶内液体Y可能是下表中的( )
A B C D X H2S SO2 CO2 Cl2 Y 浓硫酸 NaHCO3
饱和溶液Na2SO3
溶液NaHSO3
饱和溶液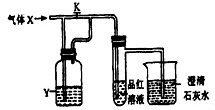
A.A、
B.B、
C.C、
D.D、难度: 中等查看答案及解析
-
Cu(NO3)2受热分解的方程式为2Cu(NO3)2=2CuO+4NO2↑+O2↑,将所得气体充满一干燥烧瓶(标准状况),再将烧瓶倒置于水中,过较长时间后,烧瓶中溶液的物质的量浓度可能为(假设烧瓶中的溶质不扩散到外面)( )
A.1/28mol/L
B.1/14mol/L
C.0mol/L
D.1/22.4mol/L难度: 中等查看答案及解析

