-
向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,充分反应后再加入稀盐酸无明显现象.下列说法正确的是( )
A.一定有锌粉剩余
B.所得溶液中一定有Zn2+、Cu2+
C.一定有银粉生成
D.所得溶液中一定有Cu2+、Ag+难度: 中等查看答案及解析
-
下列变化过程中,没有发生化学变化的是( )
A.光合作用
B.瓷碗破碎
C.食物消化
D.煤气燃烧难度: 中等查看答案及解析
-
新修订的《环境空气质量标准》增设了PM2.5监测指标.PM2.5是指大气中直径小于或等于2.5微米的颗粒物也称为可入肺颗粒物,主要来源于直接排放的工业污染物和汽车尾气等,是形成灰霾天气的最大元凶.下列做法中不合理的是( )
A.举行“地球一小时”熄灯活动
B.灰霾天出门戴N95专业口罩(过滤孔径在0.1微米左右)
C.鼓励使用太阳能热水器
D.为了减小PM2.5对环境的影响,禁止家庭使用私家车难度: 中等查看答案及解析
-
根据下列三种微粒结构示意图,所获取信息正确的是( )
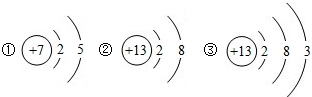
A.②③化学性质相同
B.它们表示三种元素
C.①表示的是原子,②表示的是离子
D.③表示的元素原子在化学反应中一般易得到电子难度: 中等查看答案及解析
-
配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
A. C.
C.
B.
C.
D.
难度: 中等查看答案及解析
-
2012年中央电视台播出的《舌尖上的中国》很受观众欢迎,该节目主要介绍中国的美食及其制作方法.“饮食健康”是人们普遍的生活追求,下列做法会严重危害人体健康的是( )
A.用食醋除去松花蛋的涩味
B.食品袋里充入氮气延长食品的保质期
C.在果汁中加入“塑化剂”使其口感更好
D.在煲好的鸡汤中放入适当的加碘食盐难度: 中等查看答案及解析
-
推理是一种重要的学习方法.下列推理中正确的是( )
A.含碳元素的物质燃烧都能产生CO2,在O2中燃烧生成CO2的物质都含碳元素
B.物质与氧气发生的反应都是氧化反应,则氧化反应一定要有氧气参加
C.单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
D.盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐难度: 中等查看答案及解析
-
氯气是一种有毒的气体,实验室制取氯气时,可用氢氧化钠溶液来吸收尾气,其反应原理为Cl2+2NaOH=X+NaClO+H2O,则X 的化学式及NaClO中氯元素的化合价分别为( )
A.NaCl,+1
B.H2,+3
C.HCl,+1
D.NaCl,-1难度: 中等查看答案及解析
-
已知某两种物质在光照条件下能发生化学反应,其微观示意图如下(一种小球代表一种原子),则下列说法正确的是( )

A.反应前后分子种类没有改变
B.该反应属于置换反应
C.该反应不符合质量守恒定律
D.图示中共有4种分子难度: 中等查看答案及解析
-
稀盐酸是化学实验中常用的试剂,但下列实验中,不宜使用稀盐酸的是( )
A.除去铜粉中混有的铁粉
B.除去熟石灰中的石灰石
C.区别硝酸银和硝酸钠溶液
D.检验暴露在空气中的NaOH固体是否变质难度: 中等查看答案及解析
-
取一定量的氧化铁与氧化铜的混合物,加入溶质质量分数为9.8%的稀硫酸100g,恰好完全反应生成盐和水.原混合物中氧元素的质量是( )
A.6.4g
B.3.2g
C.1.8g
D.1.6g难度: 中等查看答案及解析