-
下列反应中不属吸热反应的是( )
A.炽热的焦炭与水蒸气反应
B.氢气还原三氧化钨的反应
C.锌粒与稀H2S04反应制取H2
D.Ba(OH)2•8H2O与NH4Cl反应难度: 中等查看答案及解析
-
能说明氯的非金属性比溴强的事实是 ①共用电子对偏向:H-Cl>H-Br②酸性:HClO4>HBrO4③热稳定性:HCl>HBr④酸性:HCl<HBr( )
A.①②③
B.②③
C.①②④
D.②③④难度: 中等查看答案及解析
-
学习时通过比较、归纳,可以加深对问题的认识.下列比较或归纳一定正确的是( )
A.稳定性:NH3<PH3<AsH3
B.原子的半径>其离子半径
C.熔沸点:离子化合物>共价化合物
D.酸性:H2SO4>H3PO4>H2SiO3难度: 中等查看答案及解析
-
下列关于53131I的说法正确的是( )
A.53131I是福岛核泄漏产生的新元素
B.求算碘元素的相对原子质量必须考虑53131I的丰度
C.它的质子数和电子数之差为78
D.它的中子数和电子数之差为25难度: 中等查看答案及解析
-
下列事实与氢键有关的是( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4、SnH4熔点随着相对分子质量的增加而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱难度: 中等查看答案及解析
-
下列有关电池的叙述正确的是( )
A.氢氧燃料电池是将热能转变为电能的装置
B.氢氧燃料电池工作时氢气在正极被氧化
C.原电池反应均是氧化还原反应
D.铅蓄电池在放电过程中,负极质量减小,正极质量增加难度: 中等查看答案及解析
-
某容积固定的密闭容器中发生可逆反应:A(g)+2B(g)
C(g)+D(g),能说明反应已达到平衡状态的事实是( )
A.容器内A、B、C、D四者共存
B.VA(正)=2VB(逆)
C.容器内压强不随时间的变化而变化
D.VA(正)=VC(正)难度: 中等查看答案及解析
-
已知:下列关系正确的是( )

A.Q1+Q2>Q3
B.Q1+Q2>2Q3
C.Q1+Q2<Q3
D.Q1+Q2<2Q3难度: 中等查看答案及解析
-
参照反应Br+H2⇌HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
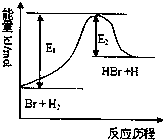
A.正反应为放热反应
B.加入催化剂,该化学反应的反应热变大
C.反应物总能量低于生成物总能量
D.升高温度可增大正反应速率,降低逆反应速率难度: 中等查看答案及解析
-
有关钢铁腐蚀与防护的说法正确的是( )
A.析氢腐蚀和吸氧腐蚀,负极均是Fe发生还原反应Fe-2e→Fe2+
B.镀层破损后,镀锡铁板的镀层仍能对铁制品起保护作用,比镀锌铁板更耐腐蚀
C.在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀难度: 中等查看答案及解析
-
下列有关物质结构的叙述正确的是( )
A.有键能很大的共价键存在的物质熔沸点一定很高
B.由离子定向移动而导电的物质一定是离子化合物
C.只含有共价键的物质不一定是共价化合物
D.在离子化合物中不可能存在非极性共价键难度: 中等查看答案及解析
-
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
2011.3.18,实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu-→Zn
⑥正极反应式:Cu+2e-═Cu2+,发生氧化反应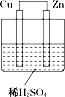
A.①②③
B.②④
C.②③④
D.③④⑤难度: 中等查看答案及解析
-
下列可逆反应达到平衡时,增大压强和升高温度使平衡移动方向相同的是( )
A.NH4HCO3(s)⇌NH3(g)+H2O(l)+CO2(g)△H>0
B.2NO2(g)⇌N2O4(g)△H<0
C.Cl2(g)+H2O(l)⇌HCl(aq)+HClO(aq)△H>0
D.2SO2(g)+O2(g)⇌2SO3(g)△H<0难度: 中等查看答案及解析
-
表是元素周期表中短周期的一部分,X、W的质子数之和为23,下列说法正确的是( )
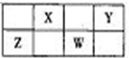
A.X元素最多可形成五种氧化物
B.Y元素的氧化物的水溶液属于强酸
C.W元素的氢化物的沸点比H2O的沸点高
D.Z的单质和Y的单质反应,其物质的量之比为1:2难度: 中等查看答案及解析
-
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应是:A(g)+xB(g)⇌2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如图所示.下列说法中正确是( )
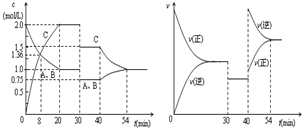
A.30min时降低温度,40min时升高温度
B.使用催化剂可以提高反应物的转化率
C.反应方程式中的x=1,正反应为吸热反应
D.8min前正反应速率大于逆反应速率难度: 中等查看答案及解析
-
一定条件下,对于可逆反应X(g)+3Y(g)⇌2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1mol•L-1、0.3mol•L-1、0.08mol•L-1,则下列判断正确的是( )
A.c1:c2<1:3
B.平衡时,Y和Z的生成速率之比为2:3
C.X、Y的转化率不相等
D.C1的取值范围为0<C1<0.14mol•L-1难度: 中等查看答案及解析
-
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍.下列说法正确的是( )
A.X的氢化物溶于水显酸性
B.Y的氧化物是离子化合物
C.Z的氢化物的水溶液在空气中存放不易变质
D.X和Z的最高价氧化物对应的水化物都是弱酸难度: 中等查看答案及解析
-
有A、B两种短周期元素,原子半径是:r(A)<r(B),且A、B两种元素原子的最外层电子数相同(选项中的m、n均为正整数),下列说法正确的是( )
A.、若B(OH)m是强碱,则A(OH)m一定为强碱
B.、若HnAOm是强酸,则B的最高价氧化物对应的水化物一定为强酸
C.、若B是金属,则A可能是非金属,若B是非金属,则A一定是非金属
D.、若HnAOm是强酸,则A元素的氢化物的水溶液一定显酸性难度: 中等查看答案及解析
-
反应CO(g)+2H2(g)CH3OH(g)过程中能量的变化如图示.下列判断正确的是( )
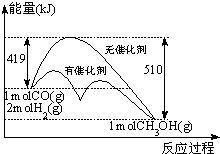
A.达到平衡时,升高温度,CO的转化率增大
B.1molCO(g)和2molH2(g)在密闭容器中反应,达平衡时,放出的热量为91KJ
C.相同条件下,1molCO(g)和2molH2(g)完全反应生成1mol液态CH3OH放出的热量等于91KJ
D.反应热取决于反应物总能量与生成物总能量的相对大小,与反应发生的条件无关难度: 中等查看答案及解析
-
在一体积不变的密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)⇌2C(g);△H<0.达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
X Y ① A的加入量 B的转化率 ② C的加入量 A的体积分数 ③ 再加入He气 A的转化率 ④ 升高温度 混合气体密度 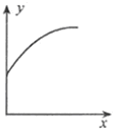
A.①
B.②
C.③
D.④难度: 中等查看答案及解析
-
X、Y、Z和R为原子序数依次递增的四种元素.其中X、Y同周期,X的最高正价是最低负价绝对值的3倍,Y、Z、R同主族,R为人体所需的微量元素.下列说法不正确的是( )
A.127R-的核外含有54个电子
B.Y、Z、R的氢化物的稳定性逐渐减弱
C.有lmolY的单质与水发生反应则转移电子的物质的量为2mol
D.在含有Z单质的水溶液中,通入足量XO2气体,则溶液由黄色变为无色难度: 中等查看答案及解析
-
一密闭容器中,400℃时存在一个化学平衡.反应进行至2min、4min时,分别只改变了某一条件,容器中四种物质的物质的量n (mol)随时间t (min)变化如图,下列说法不正确的( )
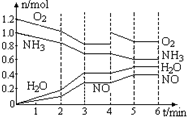
A.平衡涉及反应为4NH3+5O24NO+6H2O
B.0至3分钟气体的平均分子量在逐步减小
C.第4至5分钟平衡在右移,NH3的转化率提高
D.2min、4min时改变条件可能为降温、加入O2难度: 中等查看答案及解析