-
某同学在实验报告中写有以下实验数据:①用托盘天平称取11.7g食盐;②用量筒量取5.26mL的盐酸;③用广泛pH试纸测得某酸溶液的pH值是3.3;④滴定盐酸时用去23.00mLNaOH溶液,其中数据合理的是( )
A.①②
B.③④
C.①④
D.①③④难度: 中等查看答案及解析
-
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水.当生成1mol硝酸锌时,被还原的硝酸的物质的量为( )
A.2mol
B.1mol
C.0.5mol
D.0.25mol难度: 中等查看答案及解析
-
下列物质与常用危险化学品的类别不对应的是( )
A.H2SO4、NaOH--腐蚀品
B.CH4、C2H4--易燃液体
C.CaC2、Na--遇湿易燃物品
D.KMnO4、K2CrO7--氧化剂难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,5.6LNO和5.6LO2混合后的分子总数为0.5NA
B.1mol乙烷分子含有8NA个共价键
C.58.5g氯化钠固体中含有NA个氯化钠分子
D.在1L0.1mol/L碳酸钠溶液中阴离总数大于0.1NA难度: 中等查看答案及解析
-
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS).下列分析一定正确的是( )
A.KSP(PbS)<Kap(CuS)
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-═CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应难度: 中等查看答案及解析
-
下列各组离子,能在溶液中大量共存的是( )
A.Na+、Mg2+、AlO-、Br-
B.H十、Fe2+、SO42-、NO3-
C.K+、NH4+、CO32-、OH-
D.Ca2+、Al3+、NO3-、Cl-难度: 中等查看答案及解析
-
下列所描述的变化中不属于化学变化的是( )
A.电解质溶液导电
B.碳酸氢铵固体加热后转化为气态物质
C.干冰在空气中放置转化为气态物
D.蓝矾加热后变为白色的固体难度: 中等查看答案及解析
-
下列说法正确的是( )
A.向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色
B.欲除去氯气中少量氯化氢气体,可将此混合气体通过盛饱和食盐水的洗气瓶
C.漂白粉的有效成分是CaCl2和Ca(ClO)2,应密封保存
D.氯水经光照有气泡逸出,该气体为HCl难度: 中等查看答案及解析
-
下列叙述正确的是( )
①久置于空气中的氢氧化钠溶液,加硫酸时有气体产生
②浓硫酸可用于干燥氢气、氯化氢、碘化氢等气体,但不能干燥氨气、二氧化氮气体
③SiO2和CO2都是酸性氧化物,都能与强碱溶液反应,但不能与任何酸反应
④玻璃、水泥、水晶项链都是硅酸盐制品
⑤蔗糖炭化的演示实验中,浓硫酸既体现了其强氧化性又体现了其脱水性
⑥氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得相同的物质.
A.①④⑤
B.①⑤⑥
C.②③④
D.④⑤⑥难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A.碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O
B.溶液中NH4HSO4与NaOH等物质的量混合:NH4++HSO4-+2OH-═SO42-+NH3•H2O+H2O
C.过量的CO2通入Na[Al(OH)4]溶液中:CO2+[Al(OH)4]-═Al(OH)3↓+HCO3-
D.硫化钠溶于水中:S2-+H2O═HS-+OH-难度: 中等查看答案及解析
-
下列关于钠的化学性质叙述:
①钠与水剧烈反应生成氢氧化钠和氢气; ②钠在空气中燃烧时生成白色固体过氧化钠; ③钠与盐酸反应时先与酸反应,过量的钠再与水反应; ④钠是金属,不溶于水也不和水反应; ⑤钠可从CuSO4溶液中置换出Cu.
以上叙述正确的是( )
A.④⑤
B.②③
C.①②
D.①③难度: 中等查看答案及解析
-
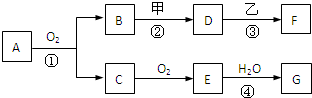
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如下的转化关系(部分产物及反应条件已略去):下列判断正确的是( )
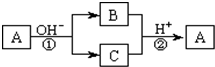
A.X元素可能为Al
B.X元素一定为非金属元素
C.反应①和②互为可逆反应
D.反应①和②不一定为氧化还原反应难度: 中等查看答案及解析
-
对于下列事实的解释错误的是( )
①蔗糖中加入浓H2SO4后出现发黑现象,说明浓硫酸具有脱水性
②浓硝酸的颜色变黄,说明浓硝酸见光易分解
③SO2气体通入溴水使溴水褪色,说明SO2具有漂白性
④常温下浓硫酸可用铁槽车储运,说明常温下浓硫酸跟铁不反应.
A.①②③④
B.③④
C.只有③
D.只有④难度: 中等查看答案及解析
-
化学实验室中常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是( )
A.定性检验SO32-,将BaCl2溶液用HNO3酸化
B.检验溶液中是否含有Fe2+时,用硝酸酸化后,加入KSCN溶液
C.为提高高锰酸钾溶液的氧化能力,用盐酸将KMnO4溶液酸化
D.检验溶液中是否含有SO42-时,在无其它阳离子干扰的条件下,所加的BaCl2溶液用盐酸酸化难度: 中等查看答案及解析
-
化学中常用类比的方法可预测许多物质的性质.如根据H2+Cl2=2HCl推测:H2+Br2=2HBr.
但类比是相对的,如根据2Na2O2+2CO2=Na2CO3+O2,类推2Na2O2+2SO2=Na2SO3+O2是错误的,应该是Na2O2+SO2=Na2SO4.
下列各组类比中正确的是( )
A.由Fe+S═FeS推测:Fe+Cl2═FeCl2
B.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO,推测:CO2+NaClO+H2O=NaHCO3+HClO
C.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
D.由Na2SO3+2HCl=2NaCl+H2O+SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+SO2↑难度: 中等查看答案及解析
-
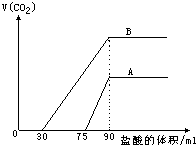
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正确的是( )
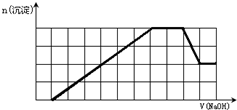
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质为Na2SO4难度: 中等查看答案及解析
-
用下列装置进行的实验,不能达到相应实验目的是( )
A.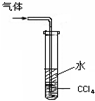
吸收尾气HCl
B.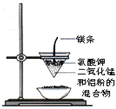
制取金属锰
C.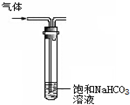
洗气除去CO2中的SO2
D.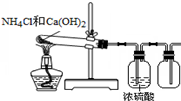
实验室制取NH3难度: 中等查看答案及解析
-
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 陈述Ⅰ 陈述Ⅱ 判断 A 碳酸钠溶液可用于治疗胃病 Na2CO3可与盐酸反应 Ⅰ对,Ⅱ对,有 B 向Na2O2的水溶液中滴酚酞变红色 Na2O2与水反应生成氢氧化钠 Ⅰ对,Ⅱ错,无 C 金属钠具有强还原性 高压钠灯发出透雾性强的黄光 Ⅰ对,Ⅱ对,有 D 过氧化钠可用于航天员的供氧 Na2O2能和CO2和H2O反应生成O2 Ⅰ对,Ⅱ对,有
A.A
B.B
C.C
D.D难度: 中等查看答案及解析