-
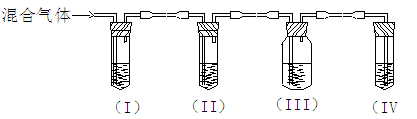
可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶
难度: 简单查看答案及解析
-
朝核问题备受人们的关注,下列关于核燃料
的说法正确的是
A.原子核内中子和质子数均为92 B.原子核外电子数为92,核内中子数为143
C.原子质量为
原子的235倍 D.
与
是两种不同的元素
难度: 中等查看答案及解析
-
下列反应中不需加热的吸热反应的是
A.锌粒与稀硫酸的反应 B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
难度: 中等查看答案及解析
-
下列表示物质结构的化学用语或模型图正确的是:
A.CO2的比例模型:
B.
的电子式
C.质量数为37的氯原子
D.
的结构示意图
[
难度: 中等查看答案及解析
-
两种气态烃组成的混合气体0.1 mol,完全燃烧后生成水3.6g,二氧化碳3.36 L(标准状况),下列说法正确的是:
A. .一定有甲烷 B一定有乙烯 C. 一定有乙烷 D.一定有丙烷
难度: 中等查看答案及解析
-
关于下图所示装置的叙述,错误的是
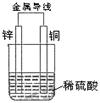
A.锌是负极,其质量逐渐减小 B.氢离子在铜表面被还原,产生气泡
C.电流从锌片经导线流向铜片 D.电子从锌片经导线流向铜片
难度: 中等查看答案及解析
-
下列关于有机物性质的说法正确的是
A.乙烯和甲烷都可以与氯气反应
B.乙烯和乙烷都可以与氢气发生加成反应
C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
D.乙烯和苯都能使酸性高锰酸钾溶液褪色
难度: 中等查看答案及解析
-
将1mol甲烷与氯气发生取代反应,待反应完全后,侧得四种有机物的物质的量相等,则消耗的氯气的物质的量为
A.1mol B.2mol C.2.5 1mol D.4mol
难度: 中等查看答案及解析
-
在元素周期表里,金属元素与非金属元素分界线附近,能找到
A. 制农药的元素 B.制半导体的元素
C.制催化剂的元素 D.制耐高温合金的元素
难度: 中等查看答案及解析
-
下列化合物中既有离子键又有共价键的是
A.KBr B. HBr C. NaOH D.N2
难度: 中等查看答案及解析
-
在条件完全相同情况下,甲、乙两同学测定反应:A2+3B2
C2的化学反应速率。甲测得v(A2)=0.5mol·(L·min)-1,乙测得v(B2)=1.5 mol·(L·min)-1,则两个学生测定的结果
A、一致 B、不一致 C、甲对,乙错 D、甲错、乙对
难度: 中等查看答案及解析
-
某元素的一种同位素X原子的质量为A,含N各中子,它与
原子组成
分子,在ag
分子中含质子的物质的量是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
关于化学键的下列叙述中,正确的是
A、离子化合物可以含共价键 B、共价化合物不可能含离子键
C、离子化合物中只含离子键 D、共价化合物中含有离子键
难度: 中等查看答案及解析
-
一定温度下,反应N2(g)+3H 2(g)
2NH3(g)达到化学平衡状态的标志是
A.混合气体的总质量不再改变
B.混合气体的平均相对分子质量不再改变
C.N2与H2的物质的量之和是NH3物质的量的2倍
D.单位时间里每增加1molN2,同时增加2mol NH3
难度: 中等查看答案及解析
-
下列排列顺序不正确的是
A、微粒半径:Na+ > K+ > Cl- > S2- B、酸性:HClO4 > H2SO4 > H3PO4 > H2SiO
C、稳定性:HI > HBr > HCl > HF 3 D、碱性:KOH > Ca(OH)2 > Mg(OH)2 > Al(OH)3
难度: 中等查看答案及解析
-
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,

难度: 中等查看答案及解析
-
.对于反应Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g) ,下列叙述不正确的

A.其反应物或生成物都能用来表示该反应的速率
B.反应过程中能量关系可用上图表示
C.若将该反应设计成原电池,锌为负极
D.若设计为原电池,当有32.5g锌溶解,正极放出标况下11.2L气体
难度: 中等查看答案及解析
-
表示阿伏加德罗常数值,下列说法中正确的是
A.1mol甲基
中含有
个电子
B.300m L2mol·L
蔗糖溶液中所含总分子数为0.6
C.标准状况下,22.4L氦气与22.4L氟气所含有的原子数均为
D.36g
分子中含有8
个共价键
难度: 中等查看答案及解析
-
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述不正确的是
元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.143
0.089
0.102
0.074
主要化合价
+2
+3
+2
+6、-2
-2
A.L2+与R2-的核外电子数相等 B..氢化物的稳定性为H2T<H2R
C M与T形成的化合物具有两性D.单质与浓度相等的稀盐酸反应的剧烈程度为Q>L
难度: 中等查看答案及解析
-
两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积是11L,下列各组混合烃中符合此条件的是:
A.C4H10、、C5H10、 B. C4H8、、C3H8 C. C4H10、、C2H4 D. CH4、、C2H4
难度: 中等查看答案及解析