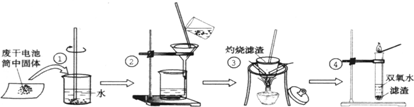
-
取少量无机盐溶液试样对其中的离子进行检验.下列判断正确的是( )
A.加入盐酸,产生白色沉淀,则试样中一定有Ag+
B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-
C.加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42-
D.加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+难度: 中等查看答案及解析
-
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A.次氯酸的电子式:
B.质量数为16的氧原子:
C.乙烯的结构简式: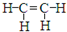
D.碳酸氢根离子的电离方程式:HCO3-+H2O⇌H3O++CO32-难度: 中等查看答案及解析
-
阿伏加德罗常数的近似值为6.02×1023,下列说法中正确的是( )
A.12g金刚石中所含共价键数目为6.02×1023
B.22.4L的HCl溶于水,溶液中H+离子数为6.02×1023
C.1molCO2与含1molNaOH的溶液反应后,溶液中离子数为6.02×1023
D.Na2O2与H2O反应,常温常压下生成16gO2,反应中转移电子数为6.02×1023难度: 中等查看答案及解析
-
对于反应O3+I-+H+-I2+O2+H2O(未配平),下列说法正确的是( )
A.O2和H2O是还原产物
B.该反应能说明O2氧化性大于I2
C.氧化产物与还原产物的物质的量之比是1:1
D.配平后的化学方程式为:2O3+2I-+4H+=I2+2O2+2H2O难度: 中等查看答案及解析
-
下列“黄色”不属于因化学反应而产生的是( )
A.硫置于水中,沉淀物呈黄色
B.久置的碘化钾溶液呈黄色
C.久置的浓硝酸呈黄色
D.鸡蛋白溶液遇浓硝酸呈黄色难度: 中等查看答案及解析
-
下列离子方程式书写正确的是( )
A.碘化亚铁溶液通入少量氯气:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2
B.苯酚钠溶液通入少量二氧化碳:C6H5O-+CO2+H2O=C6H5OH+CO32-
C.碳酸氢钠溶液加入少量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32-
D.硫酸氢铵溶液加入足量氢氧化钡溶液:2NH4++Ba2++SO42-+2OH-=BaSO4↓+2NH3•H2O难度: 中等查看答案及解析
-
铅蓄电池在现代生活中具有广泛的应用.已知铅蓄电池的电解质溶液为H2SO4溶液,其充电、放电按下式进行:
Pb+PbO2+2H2SO42PbSO4+2H2O,有关该电池的说法正确的是( )
A.充电时化学能转化为电能
B.放电时溶液中的H+向负极移动
C.充电时电池的正极与电源的正极相连
D.放电时负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42-难度: 中等查看答案及解析
-
下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ•mol-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ•mol-1,则CH3OH的燃烧热为192.9kJ•mol-1
C.H2(g)的燃烧热是285.8kJ•mol-1,则2H2O(g)=2H2(g)+O2(g);△H=+571.6kJ•mol-1
D.葡萄糖的燃烧热是2800kJ•mol-1,则1/2C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400kJ•mol-1难度: 中等查看答案及解析
-
常温下,0.1mol•L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是( )
A.该溶液中水电离出的c(H+)=1×10-10mol•L-1
B.该溶液中c(H+)+c(A-)+c(HA)=0.1mol•L-1
C.该溶液与0.05mol•L-1NaOH溶液等体积混合后:c(A-)>c(Na+)>c(OH-)>c(H+)
D.向该溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大难度: 中等查看答案及解析
-
将一定量A、B装入容积为1L的恒温密闭容器中,发生反应:2A(s)+bB(g)⇌cC(g),1min时达到平衡,C的浓度为x mol•L-1.若保持温度不变,将密闭容器的容积压缩为原来的
,重新达到平衡后,C的浓度为2.5x mol•L-1.下列说法正确的是( )
A.化学计量数的关系:b<c
B.容器的容积减小后,该反应的逆反应速率减小
C.若保持温度和容器的容积不变,充入氦气(不参与反应),平衡不发生移动
D.原容器中用B的浓度变化表示该反应在1min内的速率为mol•L-1•min-1
难度: 中等查看答案及解析
-
一次性使用的聚苯乙烯(
)材料易造成“白色污染”,其替代物聚乳酸(
)是由乳酸(
)聚合而成的,聚乳酸可在乳酸菌的作用下降解.下列说法中正确的是( )
A.聚苯乙烯的单体为
B.聚苯乙烯与聚乳酸的聚合方式相似
C.聚苯乙烯和聚乳酸均为纯净物
D.乳酸可发生消去反应难度: 中等查看答案及解析
-
在下列条件下,一定能大量共存的离子组是( )
A.在透明的溶液中:Fe2+、H+、I-
B.在pH=1的溶液中:Cl-、NH4+、ClO-
C.滴加KSCN试剂呈红色的溶液中:K+、SO32-、HCO3-
D.在由水电离出的c(H+)×c(OH-)=1×10-24的溶液中:CH3COO-、F-、Na+难度: 中等查看答案及解析
-
下列各组物质不属于同分异构体的是( )
A.2,2-二甲基丙醇和2-甲基丁醇
B.甲基丙烯酸和甲酸丙酯
C.2-甲基丁烷和戊烷
D.邻氯甲苯和对氯甲苯难度: 中等查看答案及解析
-
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中产物中一定不存在同分异构体的是( )
A.邻羟基苯甲酸与NaHCO3溶液反应
B.2-氯丁烷(CH3CH2CClHCH3)与NaOH乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D.异戊二烯(CH2=C(CH3)CH=CH2)与等物质的量的Br2发生加成反应难度: 中等查看答案及解析
-
茉莉醛具有浓郁的茉莉花香,其结构简式为:
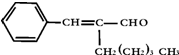 ,关于茉莉醛的下列表述不正确的是
,关于茉莉醛的下列表述不正确的是
( )
A.难溶于水
B.属于芳香烃
C.在一定条件下能发生氧化反应
D.在一定条件下能生成高分子化合物难度: 中等查看答案及解析