-
常温下,盐酸与氨水混合,所得溶液pH=7,则此溶液中的关系正确是( )
A.c(NH4+)<c(Cl-)
B.c(NH4+)=c(Cl-)
C.c(NH4+)>c(Cl-)
D.无法确定c(NH4+)与c(Cl-)难度: 中等查看答案及解析
-
向三份1mol/L CH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl3固体(忽略溶液体积变化),则CH3COO-浓度的变化依次为( )
A.减小、增大、减小
B.增大、减小、减小
C.减小、增大、增大
D.增大、减小、增大难度: 中等查看答案及解析
-
下列关于金属的腐蚀说法正确的是( )
A.一般来说,金属发生化学腐蚀的速率比电化学腐蚀速率要快
B.保护地下钢管不受腐蚀,可使它连接直流电源的负极
C.钢铁发生析氢腐蚀时,正极的电极反应式为:2H2O+O2+4e-=4OH-
D.轮船底部放一块锌块,所采用的防腐方法为牺牲阴极的阳极保护法难度: 中等查看答案及解析
-
下列过程或现象与盐类水解无关的是( )
A.纯碱溶液去油污
B.加热稀醋酸溶液其pH 稍有减小
C.实验室配置FeCl3溶液时,加入少量稀盐酸,以防止溶液浑浊
D.水中加入明矾可以净化水难度: 中等查看答案及解析
-
下列过程中需要通电才可以进行的是( )
①电离 ②电解 ③电镀 ④电化学腐蚀.
A.①②③
B.②③④
C.②③
D.全部难度: 中等查看答案及解析
-
已知水的电离方程式:H2O⇌H++OH-.下列叙述中,正确的是( )
A.升高温度,KW增大,pH不变
B.向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低
C.向水中加入少量硫酸,c(H+)增大,KW不变
D.向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低难度: 中等查看答案及解析
-
有关AgCl的溶解沉淀平衡的说法中,不正确的是( )
A.达到沉淀溶解平衡时,AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Cl-
C.升高温度时,AgCl的溶解度增大
D.向AgCl饱和溶液中,加入NaCl固体,会析出AgCl固体难度: 中等查看答案及解析
-
已知蓄电池在充电时作电解池,放电时作原电池.铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”.关于标有“+”的接线柱,下列说法中正确的是( )
A.充电时作阳极,放电时作正极
B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时放正极难度: 中等查看答案及解析
-
向纯水中加入少量的硫酸氢钠(溶液温度不变),则溶液的( )
A.pH值升高
B.酸性增强
C.水的离子积增大
D.c (OH-)不变难度: 中等查看答案及解析
-
如图,横坐标表示加水量,纵坐标表示导电能力,能表示冰醋酸(即无水醋酸)加水稀释的图是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
下列属于正确的水解离子方程式的是( )
A.NH4++H2ONH3•H2O+H+
B.H2O+H2OH3O++OH-
C.CO32-+2H2OH2CO3+2OH-
D.Fe3++3H2OFe(OH)3↓+3H+
难度: 中等查看答案及解析
-
下列关于电解质的说法正确的是( )
A.强电解质溶液的导电性一定比弱电解质溶液的导电性强
B.强电解质都是离子化合物,而弱电解质都是共价化合物
C.强电解质在稀的水溶液中全部以离子的形态存在
D.水溶液中导电能力差的电解质一定是弱电解质难度: 中等查看答案及解析
-
能说明醋酸是弱电解质的是( )
A.中和10mL 1mol/L CH3COOH溶液需要10ml 1mol/L NaOH溶液
B.用食醋可以除热水瓶内的水垢
C.pH=2的醋酸溶液稀释1000倍后pH小于5
D.用浓H2SO4和醋酸钠固体共热可制得醋酸难度: 中等查看答案及解析
-
常温下,某溶液中由水电离出的c(H+)=10-12mol/L,则该溶液中一定不能大量存在的离子组是( )
A.Cu2+、NO3-、Cl-、Na+
B.Ca2+、HCO3-、Cl-、K+
C.NH4+、Mg2+、NO3-、SO42-
D.Cl-、SO42-、K+、Na+难度: 中等查看答案及解析
-
如图所示,各烧杯中均盛有海水,铁在其中被腐蚀由快到慢的顺序为( )

A.②①③④
B.④③①②
C.④②①③
D.③②④①难度: 中等查看答案及解析
-
用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是( )
A.CuCl2 (CuO)
B.NaOH (NaOH)
C.CuSO4 (CuO)
D.NaCl (NaOH)难度: 中等查看答案及解析
-
下列各装置中铜电极上能产生气泡的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
右图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽.接通电路后发现B上的c点显红色.为实现铁上镀锌,接通K后,使c、d两点短路.下列叙述正确的是( )

A.a为直流电源的负极
B.c极发生的反应为2H++2e-═H2↑
C.f电极为锌板
D.e极发生还原反应难度: 中等查看答案及解析
-
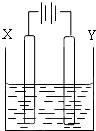
右图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是( )
a极板 b极板 X电极 电解质溶液 A 锌 石墨 负极 CuSO4 B 石墨 石墨 负极 NaOH C 银 铁 正极 AgNO3 D 铜 石墨 负极 CuCl2
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料的说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10+13O2=8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+2e-=2O2-
D.通入丁烷的一极是正极,电极反应为:C4H10+26 e-+13 O2-=4 CO2+5 H2O难度: 中等查看答案及解析