-
下列关于物质的性质和用途的说法中,不正确的是( )
A
B
C
D
氧化铁

带玻璃塞的试剂瓶

铁罐车

铝制饭盒

可用作红色颜料
可用于盛放
氢氧化钠溶液
可用于运输浓硫酸
不宜长时间存放酸性或碱性的食物
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列说法不正确的( )
A. 玛瑙、水晶、钻石等装饰品的主要成分不相同
B. 铁粉可作食品袋内的脱氧剂
C. 漂白液、漂白粉、漂粉精的成分尽管不同,但漂白原理是相同的
D. 浓硫酸可刻蚀石英制艺术品
难度: 简单查看答案及解析
-
下列解释实验事实的方程式不正确的是( )
A. 用NaS处理含Hg2+的废水:Hg2++S2-=HgS↓
B. 用氢氧化钠溶液去除铝条表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O
C. 向硫酸铜溶液中加入过氧化钠:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
D. 向石灰乳中通入氯气制取漂白粉: 2OH-+Cl2= Cl-+ ClO-+H2O
难度: 中等查看答案及解析
-
重水(D2O)是重要的核工业原料,下列说法错误的是( )
A. 1mol D2O含有10NA个电子 B. 1H与D互称同位素
C. H2O与D2O互称同素异形体 D. 1H→D通过化学变化不能实现
难度: 简单查看答案及解析
-
下列关于第ⅠA族和第ⅦA族元素的说法正确的是( )
①第ⅠA族元素都是金属元素
②第ⅠA族元素都能形成+1价的离子
③第ⅦA族元素的最高正价都为+7
④第ⅦA族元素简单气态氢化物的热稳定性逐渐减弱
A. ①③ B. ②③ C. ②④ D. ③④
难度: 中等查看答案及解析
-
下列排列顺序错误的是( )
A. 金属性 Rb>K>Mg>Al B. 非金属性 P>S>Cl>F
C. 稳定性 SiH4<PH3<H2S<HF D. 半径 Na>P>O>F
难度: 中等查看答案及解析
-
硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图为:
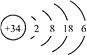 。下列说法不正确的是( )
。下列说法不正确的是( )A. 该元素处于第四周期第ⅥA族 B. SeO2既有氧化性又有还原性
C. 该原子的质量数为34 D. 酸性:HBrO4 > H2SeO4
难度: 中等查看答案及解析
-
有一无色溶液,可能含有Fe3+、K+、Al3+、Mg2+、NH4+、Cl-、SO42-、HCO3-、MnO4-中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量的Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的是( )
A. 肯定有Al3+、Mg2+、NH4+ B. 肯定有Al3+、Mg2+、HCO3-
C. 肯定有K+、MnO4- D. 肯定有Al3+、Mg2+、SO42-
难度: 中等查看答案及解析
-
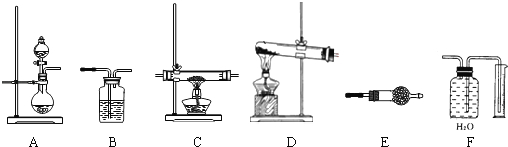
下列装置能达到实验目的是( )
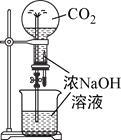
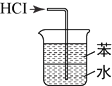
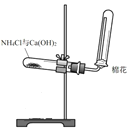
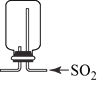
图1
图2
图3
图4
A. 利用图1装置进行喷泉实验
B. 利用图2装置吸收HCl气体,并防止倒吸
C. 利用图3装置制备NH3
D. 利用图4装置收集SO2气体
难度: 中等查看答案及解析
-
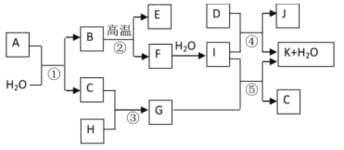
有X、Y、Z、W、M五种原子序数依次增大的前20号元素,其中X、M同主族,M原子有4个电子层;Z2+与Y2-具有相同的电子层结构,W是地壳中含量最多的金属,X与M的原子序数之和等于Y与Z的原子序数之和。下列叙述不正确的是( )
A. 原子半径大小:M>Z>W
B. W的氧化物可与M的氧化物的水化物反应
C. X有多种同素异形体,而Y不存在同素异形体
D. 含M元素物质的焰色反应(透过蓝色钴玻璃)为紫色
难度: 中等查看答案及解析
-
短周期主族元素 W、 X、 Y、 Z 的原子序数依次增大,W的最外层电子数是内层电子数的3倍,X所在的周期数是最外层电子数的3倍,由 W、 X、 Y 三种元素形成的一种盐溶于水后,加入盐酸,产生的无色气体能使品红褪色。下列说法正确的是( )
A. W 与 X 可形成至少两种化合物
B. X 的简单离子与 Z 的简单离子具有相同的电子层结构
C. 最高价氧化物对应水化物的酸性: Y>Z
D. 简单气态氢化物的稳定性: W<Y
难度: 中等查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期主族元素,其中Y、W同主族,W的最外层电子数为Z的2倍,m是X与W形成的化合物,n是Y与W形成的化合物,m、n有如图所示的转化关系,p在常温下为常见的液态化合物,q是W的单质。下列说法不正确的是( )
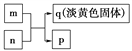
A. 原子半径:Z>W>Y>X
B. 简单氢化物的稳定性:Y>W
C. Z与Y形成的化合物具有两性
D. W的最高价氧化物对应的水化物是一种弱酸
难度: 中等查看答案及解析
-
利用下图装置可以进行实验并能达到实验目的的是( )
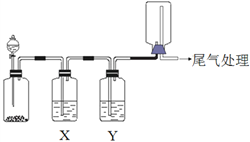
选项
实验目的
X中试剂
Y中试剂
A
用MnO2和浓盐酸制取并收集纯净干燥的Cl2
饱和食盐水
浓硫酸
B
用Cu与稀硝酸制取并收集纯净干燥的NO
水
浓硫酸
C
验证Na2SO3和浓硫酸反应的产物的性质
品红溶液
KMnO4溶液
D
CaCO3和稀盐酸制取并收集纯净干燥的CO2
饱和Na2CO3溶液
浓硫酸
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
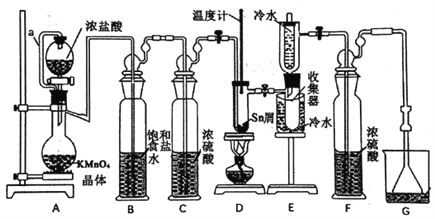
碳跟浓硫酸共热产生的混合气体X和铜跟浓硝酸反应产生的混合气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
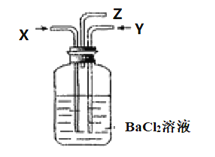
A. 洗气瓶中产生的沉淀是BaCO3
B. 在Z导管出来的气体中无CO2
C. 洗气瓶中产生的沉淀是BaSO3
D. 在Z导管口有红棕色气体
难度: 中等查看答案及解析
-
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是( )
A. 滴加KI溶液时,KI被氧化,CuI是氧化产物
B. 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
C. 滴加KI溶液时,转移1mole-时生成0.5mol白色沉淀
D. 上述实验条件下,物质的氧化性:Cu2+>I2>SO2
难度: 中等查看答案及解析
-
将25.6克的铜完全溶于适量的浓硝酸中,收集到氮的氧化物(NO2、N2O4、NO)的混合气,这些混合气恰好能被250ml 2mol/L NaOH溶液完全吸收,生成NaNO2和NaNO3的盐溶液,则其中NaNO3的物质的量为
A、0.1 mol B、0.2 mol C、0.3mol D、0.4 mol
难度: 困难查看答案及解析