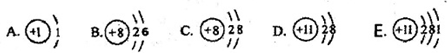-
月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为( )
A.+1
B.+2
C.+3
D.+4难度: 中等查看答案及解析
-
下列关于“燃烧和灭火”的叙述正确的是( )
A.档案室着火用泡沫灭火器灭火
B.炒菜时油锅着火,立即盖上锅盖
C.只有含碳元素的物质才能燃烧
D.只要温度达到可燃物的着火点,可燃物就能燃烧难度: 中等查看答案及解析
-
在人类的生产和生活中,不会造成空气污染的是( )
A.煤炭燃烧
B.植物的光合作用
C.石油化工厂排出的废气
D.汽车尾气难度: 中等查看答案及解析
-
有X、Y、Z三种金属,将三种金属分别浸入稀硫酸中,Y溶解并放出氢气,X、Z不溶解;将X浸入Z的硫酸盐溶液中,在X的表面有Z析出.则三种金属的活动性由强到弱排列顺序正确的是( )
A.X>Y>Z
B.Y>X>Z
C.Y>Z>X
D.X>Z>Y难度: 中等查看答案及解析
-
下列“家庭小实验”不能达到预期目的是( )
A.用柠檬酸、果汁、白糖、水、小苏打等制汽水
B.用空塑料瓶、小卵石、石英沙、活性炭、膨松棉、纱布等制作简易净水器
C.用酒精浸泡捣烂的某些植物的花瓣可制酸碱指示剂
D.向洗净的碎鸡蛋壳中加入食盐水可制二氧化碳难度: 中等查看答案及解析
-
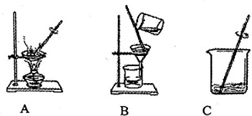
下列变化中,属于化学变化的是( )
A.
水的电解
B.
水的沸腾
C.
捣碎胆矾
D.
干冰升华难度: 中等查看答案及解析
-
化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用.下列说法正确的是( )
A.铁元素是人体必需的常量元素,主要存在血液中
B.熟石灰可以改良酸性土壤,但不能和硫酸铵混合使用
C.塑料都有热塑性,可以反复加工,多次使用,有会造成“白色污染”
D.木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关难度: 中等查看答案及解析
-
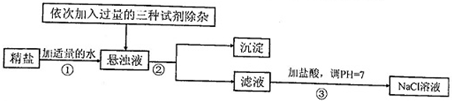
除去下列物质中的杂质所选用的试剂及操作方法不正确的一组是( )
物质 所含杂质 除去杂质的方法 A Cu(NO3)2溶液 (AgNO3溶液) 加入过量的铜粉,过滤 B N2气体 (O2) 将气体缓缓通过灼热的铜网 C Cu0 (Cu) 过量的稀硫酸溶液、过滤 D KNO3 (NaCl) 热水、降温结晶、过滤
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
如图表示治理汽车尾气所涉及反应的微观过程.下列说法正确的是( )

A.图中有两种单质和两种氧化物
B.反应物和生成物均含有毒气体
C.生成物的分子个数比为1:1
D.生成单质与化合物的质量比为7:22难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.不同元素本质的区别是原子的最外层电子数不同
B.水通电生成氢气和氧气,在化学反应中分子可分,原子不能再分
C.符号“Cu”既能表示该种元素,又能表示该元素的一个原子,还能表示该种物质
D.二氧化碳能灭火而一氧化碳能燃烧,二氧化碳和一氧化碳的分子构成不同难度: 中等查看答案及解析
-
工业酒精中含有甲醇.关于甲醇的下列叙述不正确的是( )
A.甲醇是由1个碳原子、4个氢原子和一个氧原子构成的
B.甲醇中氧元素的质量分数为50%
C.甲醇的相对分子质量为32g
D.48g甲醇中含18g碳元素难度: 中等查看答案及解析
-
下表是某同学用两种方法鉴别物质的情况,其中两种方法都正确的是( )
选项 需要鉴别的物质 方法和所加试剂 方法一 方法二 A 碳酸钠溶液和氢氧化钠溶液 滴加无色酚酞溶液 滴加氯化钡溶液 B 一氧化碳和二氧化碳 通入紫色的石蕊溶液 通入澄清的石灰水 C 硝酸铵和硫酸钾 加氢氧化钙研磨 加适量水观察是否溶解 D 稀盐酸和氢氧化钠溶液 加入碳酸钠溶液 加入硫酸铜溶液
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下表提供的四组物质符合图示相连物质间在一定条件下可以发生反应的是( )
甲 乙 丙 丁 A CO O2 H2SO4 CuO B Mg HCl CuSO4 NaOH C KOH SO3 NaOH CuSO4 D Na2CO3 Ca(OH)2 HCl CaCl2 
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列对比实验不能达到实验目的是( )
选项 实验目的 实验设计 实验一 实验二 A 探究铁、铜、银三种金属的活动性顺序 将铁丝放入2mL10%的硫酸铜溶液中 将银丝放入2mL10%硫酸铜溶液中 B 催化剂对化学反应速率的影响 将带火星的木条伸入装有5mL5%过氧化氢溶液的试管中 将带火星的木条伸入装有少量二氧化锰和5mL5%过氧化氢溶液的试管中 C 酸雨危害的模拟实验 将植物嫩叶浸泡10mL蒸馏水中 取10mL蒸馏水,通入过量二氧化硫气体,再将植物嫩叶浸泡其中 D 铁生锈是铁与水和氧气共同作用的结果 将铁钉放入装有水的试管中,使铁钉一半被水淹没 将铁钉放入干燥的试管中并将试管口密封
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
有反应:8A+3B2=C2+6D(其中A、D是化合物,B2、C2是单质).若13.6g A与21.3g B2恰好完全反应,生成32.1g D,已知C2的相对分子质量为28,则B的相对原子质量为( )
A.14
B.16
C.32
D.35.5难度: 中等查看答案及解析