-
化学与生活、社会发展细细相关,下列有关说法不正确的是
A.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.维生素C具有还原性,在人体内起抗氧化作用
难度: 简单查看答案及解析
-
如图表示的一些物质或概念间的从属关系中不正确的是
X
Y
Z
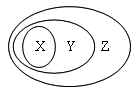
A
氧化物
化合物
纯净物
B
电解质
盐
化合物
C
胶体
分散系
混合物
D
碱性氧化物
金属氧化物
氧化物
难度: 中等查看答案及解析
-
下列有关胶体的说法中,不正确的是
A.胶体、溶液、浊液的分类依据是分散质微粒直径大小
B.“卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关
C.向1mol•L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体
D.可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体
难度: 中等查看答案及解析
-
NA代表阿伏伽德罗常数,下列说法中正确的是
A.在同温同压时,相同体积的任何气体单质所含的原子数目相同
B.在标准状况下,22.4L水中所含的分子数为
C.在常温常压下,11.2L氮气所含的原子数是NA
D.34g氨气所含质子数目为20NA
难度: 中等查看答案及解析
-
下列各组数据中,前者刚好是后者两倍的是
A.2molH2O的摩尔质量和1molH2O的摩尔质量
B.200mL 1mol/L氯化钙溶液中c(Cl-)和100mL 2 mol/L氯化钾溶液中c(Cl-)
C.64gSO2中氧原子数和标准状况下22.4LCO中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
难度: 中等查看答案及解析
-
下列配制的溶液浓度偏高的是
A.配制盐酸溶液,用量筒量取盐酸时俯视刻度线
B.配制盐酸溶液定容时,仰视容量瓶
C.称量40gNaOH配制0.20mol/LNaOH溶液500mL时,砝码错放左盘
D.配制NaOH溶液时,溶液未经冷却即注入容量瓶并定容至刻度线
难度: 中等查看答案及解析
-
同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是
①分子数比为11:16 ②密度比为11:16 ③体积比为16:11 ④原子个数比为11:16
A.①③ B.①④ C.②③ D.②④
难度: 中等查看答案及解析
-
现有以下混合液体:①汽油和氯化钠溶液 ②乙醇与水 ③氯化钠溶液和单质溴,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
常温下,某溶液中可以发生反应:X+2Y3+═2Y2+X2+,则①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性大于X2+的氧化性要强。上述叙述中正确的是
A.②④⑥ B.①③④ C.①③⑤⑥ D.②⑤
难度: 中等查看答案及解析
-
下列离子方程式改写成化学方程式正确的是
A.Cu2++2OH-=Cu(OH)2↓;CuCO3+2NaOH=Cu(OH)2↓+Na2CO3
B.CO32-+2H+=CO2↑+H2O;BaCO3+2HCl=BaCl2+CO2↑+H2O
C.CO32-+Ca2+=CaCO3↓;Ca(NO3)2+NaCO3=CaCO3↓+NaNO3
D.H++OH-=H2O;2KOH+H2SO4=K2SO4+2H2O
难度: 中等查看答案及解析
-
下列各组离子在溶液中能大量共存的是
A.Na+、Al3+、Cl-、SO42- B.Cu2+、Cl-、NO3-、OH-
C.Ca2+、Na+、CO32-、NO3- D.H+、SO42-、NO3-、OH-
难度: 中等查看答案及解析
-
下列说法不正确的是
①将BaSO4放入水中不能导电,所以BaSO4是非电解质;②氨溶于水得到的氨水能导电,所以氨水是电解质;③熔融态的HCl可以导电;④固态NaCl不导电,熔融态的NaCl也不导电⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
A①④ B.①④⑤ C.①②③④ D.①②③④⑤
难度: 中等查看答案及解析
-
以下对电子转移的方向和数目的表示正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是
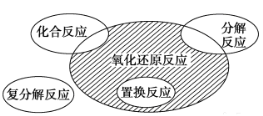
A.CuSO4+Mg==Cu+MgSO4
B.2NaHCO3
Na2CO3+H2O+CO2↑
C.2Na2O2+2CO2==2Na2CO3+O2↑
D.4Fe(OH)2+O2+2H2O==4Fe(OH)3
难度: 中等查看答案及解析
-
如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是
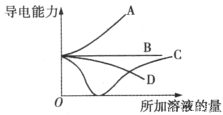
A.曲线A表示NaOH溶液中滴加稀盐酸
B.曲线B表示CH3COOH溶液中滴加KOH溶液
C.曲线C表示Ba(OH)2溶液中滴加稀硫酸
D.曲线D表示Cu(OH)2悬浊液中滴加HNO3溶液
难度: 困难查看答案及解析
-
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是
A.①④②⑤③ B.④①②⑤③ C.②⑤④③① D.⑤②④①③
难度: 中等查看答案及解析
-
只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是
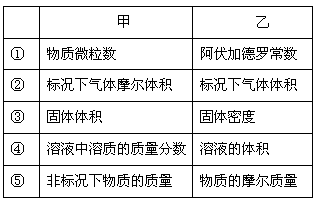
A.③ B.③④ C.②③④ D.③④⑤
难度: 中等查看答案及解析
-
将amol/L Al2(SO4)3和钾离子浓度为2bmol/L的K2SO4混合溶液500mL加水稀释到2L,则稀释后的溶液中SO42-的浓度为
A.(a+b)/4 mol/L B.4(3a+b) mol/L C.4(a+b) mol/L D.(3a+b)/4 mol/L
难度: 中等查看答案及解析
-
在xR2++yH++O2=mR3++nH2O的离子方程式中,对化学计量数m和R2+、R3+,判断正确的是
A.m=y,R3+是还原剂 B.m=4,R2+是还原剂
C.m=2,R3+是氧化剂 D.m=2y,R2+被氧化
难度: 中等查看答案及解析
-
将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg•cm-3,则该盐酸的物质的量浓度是
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 困难查看答案及解析