-
下列物质的主要成分属于氧化物的是( )
A. 钻石(C) B. 食盐(NaCl) C. 水晶(SiO2) D. 钟乳石(CaCO3)
难度: 简单查看答案及解析
-
““群众利益无小事,食品安全是大事”下列关于生活和健康常识的说法不正确的是( )
A. 福尔马林不可用于水产品保鲜
B. 含亚硝酸钠的工业用盐不能用于腌制食品
C. 用地沟油烹饪的食物危害人体健康
D. 可用硫磺熏制白木耳、粉丝等食品
难度: 中等查看答案及解析
-
下列生活用品所使用的主要材料,属于有机合成材料的是

A.青花瓷瓶 B.塑料水杯 C.纯棉毛巾 D.不锈钢锅
难度: 简单查看答案及解析
-
(2011龙岩)科学家发现食用富含维生素的食物具有较好的防电磁辐射的功能.下列食物中富含维生素的是( )
A. 胡萝卜
B. 牛奶
C. 豆腐
D. 米饭
难度: 简单查看答案及解析
-
依据国家相关法律规定,自2011年5月1日起,机动车驾驶员醉驾将受到刑事处罚。 检测驾驶员是否酒后驾车,可用一种装有重铬酸钾(K2Cr2O7)的仪器。在K2Cr2O7中铬元素(Cr)的化合价是( )
A. +2 B. +3 C. +6 D. +7
难度: 中等查看答案及解析
-
日常生活常接触到“含氟牙膏”、“高钙牛奶”、“碘盐”、“富硒茶叶”、“加铁酱油”等用品,这里的氟、钙、碘、硒、铁指的是( )
A. 单质 B. 原子 C. 元素 D. 离子
难度: 简单查看答案及解析
-
长期施用(NH4)2SO4化肥的土壤容易酸化。下列说法不正确的是( )
A.(NH4)2SO4属于氮肥
B.(NH4)2SO4的水溶液能使酚酞溶液显红色
C.不宜长期施用(NH4)2SO4化肥
D.(NH4)2SO4化肥不能与碱性物质混合施用
难度: 简单查看答案及解析
-
下图表示的是身边一些物质在常温时的近似pH。下列叙述不正确的是( )

A. 橘子汁的酸性比萝卜汁的酸性弱 B. 鸡蛋清呈碱性
C. 草木灰水呈碱性 D. 柠檬汁能使紫色石蕊溶液变红
难度: 简单查看答案及解析
-
用分子的观点解释下列现象,不合理的是
A. 食物变质——分子本身发生了变化 B. 汽油挥发——分子大小发生了变化
C. 热胀冷缩——分子间间隔改变 D. 花香四溢——分子做扩散运动
难度: 简单查看答案及解析
-
下列有关物质性质与用途的对应关系错误的是( )
A. 稀有气体的惰性——用来填充灯泡 B. 金刚石的硬度大——用于防毒面具
C. 氢气的可燃性——作火箭的燃料 D. 氢氧化钠易潮解———作某些气体干燥剂
难度: 中等查看答案及解析
-
你经常做家庭小实验吗?根据你的经验,下列家庭小实验不成功的是( )
A. 通过把水煮沸可以降低水的硬度
B. 用食盐水除去水瓶中的水垢
C. 用食醋和小苏打制取二氧化碳
D. 用花瓣制作指示剂,检验纯碱溶液的酸碱性
难度: 中等查看答案及解析
-
下列物质溶于水时,溶液温度明显降低的是 ( )
A. 硝酸铵 B. 氯化钠 C. 浓硫酸 D. 氢氧化钠
难度: 简单查看答案及解析
-
如右图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是
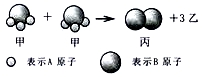
A、反应生成的丙物质属于单质
B、参加反应的甲物质属于化合物
C、该反应中原子的种类发生了改变
D、根据质量守恒定律可推知,1个乙分子中含有2个A原子
难度: 中等查看答案及解析
-
下列化学方程式的表达一定不正确的是 ( )
A. 2Fe + 6HCl = 2FeCl3 + 3H2↑ B. BaCl2+ CuSO4 = BaSO4↓+ CuCl2
C. CO2+ 2NaOH = Na2CO3 + H2O D. Ca(OH)2 + Na2CO3 = CaCO3↓+ 2NaOH
难度: 中等查看答案及解析
-
下列图标中,在商场、医院、车站等公共场所最常见的是( )
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
.下列各组现象所伴随的变化属于化学变化的是
A. 蜡烛燃烧 B. 滴水成冰 C. 电灯发光 D. 汽油挥发
难度: 简单查看答案及解析
-
下列物质暴露在空气中质量会减轻的是
A.浓盐酸 B.铁粉 C.生石灰 D.石灰水
难度: 中等查看答案及解析
-
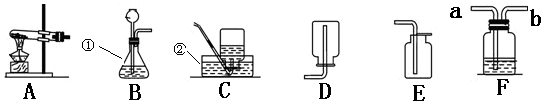
下列图示实验基本操作中错误的是( )
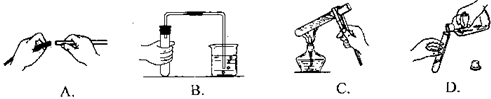
A. A B. B C. C D. D
难度: 简单查看答案及解析