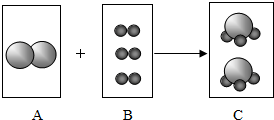-
在食盐中加入KIO3有益于防治地方性甲状腺肿大,检验食盐中是否含有碘酸钾,可利用化学反应:5x+KIO3+3H2SO4═3K2SO4+3I2+3H2O,其中x的化学式为( )
A.HI
B.KI
C.I2O2
D.HIO3难度: 中等查看答案及解析
-
水是生命之源,下列各种水属于纯净物的是( )
A.井水
B.自来水
C.蒸馏水
D.矿泉水难度: 中等查看答案及解析
-
长期受电磁辐射可引起人头昏、头痛、失眠等症,科学家发现富含维生素的食物具有较好的防辐射损伤功能.下列食物中富含维生素C的是( )
A.油菜
B.牛奶
C.豆腐
D.米饭难度: 中等查看答案及解析
-
下列变化过程中包含化学变化的是( )
A.冰雪融化
B.空气液化
C.干冰升华
D.光合作用难度: 中等查看答案及解析
-
厨房中的下列物质与水混合后,不能形成溶液的是( )
A.植物油
B.白糖
C.味精
D.食盐难度: 中等查看答案及解析
-
化石燃料是不可再生能源,在地球上的蕴藏量是有限的,开发和有效利用新能源迫在眉睫.下列能源中属于新能源的是
( )
A.煤
B.石油
C.太阳能
D.天然气难度: 中等查看答案及解析
-
下列实验操作中正确的是( )
A.
B.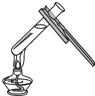
C.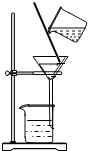
D.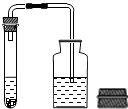
难度: 中等查看答案及解析
-
掌握化学知识有助于我们更健康地生活.下列做法正确的是( )
A.随意使用各种塑料袋包装食品
B.不吃或少吃含亚硝酸盐的熟食制品
C.用甲醛浸泡海鲜产品来延长食品保质期
D.霉变的大米用水泡去表面的霉点后食用难度: 中等查看答案及解析
-
下列结构示意图所表示的微粒,属于同种元素的是( )
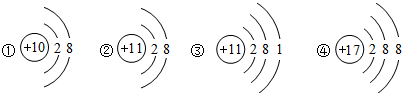
A.①②
B.②③
C.③④
D.①②④难度: 中等查看答案及解析
-
作为2008年北京奥运会足球比赛的分赛场,沈阳奥体中心体育场宛如水晶皇冠般璀璨地闪耀在浑河南岸.场馆建设中使用了大量的钢筋,下列有关钢筋的说法中不正确的是( )
A.钢筋是混合物
B.钢筋属于金属材料
C.钢筋的韧性优于生铁
D.钢筋混凝土就是钢筋和混凝土的合成材料难度: 中等查看答案及解析
-
小强家的仓库里存有少量无标签但密封良好的化肥.为了确定该化肥的成分,他取少量化肥与熟石灰粉末混合、研磨,闻到刺激性气味.由此判断该化肥为( )
A.氯化铵
B.碳酸钾
C.硫酸钾
D.硝酸钠难度: 中等查看答案及解析
-
一次性就能将澄清石灰水、稀硫酸、食盐水三种溶液区分开的试剂是( )
A.二氧化碳气体
B.无色酚酞试液
C.氯化钡溶液
D.碳酸钠溶液难度: 中等查看答案及解析
-
小刚同学在做有关NaOH溶液性质的实验时,向NaOH溶液中滴加过量的CuSO4溶液.下列图象中能正确表示其变化过程的是( )
A.
B.
C.
D.难度: 中等查看答案及解析