-
“金银铜铁锡”俗称五金,在这五种金属中,有一种金属与其他四种金属的盐溶液都能发生反应,这种金属是( )
A.金
B.铜
C.铁
D.锡难度: 中等查看答案及解析
-
将下列四种家庭常用的调味品分别放入水中,不能形成溶液的是( )
A.芝麻油
B.食盐
C.味精
D.蔗糖难度: 中等查看答案及解析
-
除去下列物质中的杂质,所用的试剂和方法不正确的是( )
A.除去二氧化碳中混有的一氧化碳可以用点燃的方法
B.除去氯化钾中混有的二氧化锰可以用溶解、过滤、蒸发的方法
C.除去铜粉中混有的锌粉可以用加入过量的稀盐酸、过滤、洗涤、烘干的方法
D.除去生石灰中混有的碳酸钙可以用高温煅烧的方法难度: 中等查看答案及解析
-
下列现象和做法,仅涉及物理变化的是( )
A.
绿色植物光合作用
B.
世博会开幕燃放烟花
C.
电解水探究水的组成
D.
相互划刻比较硬度难度: 中等查看答案及解析
-
芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的.下面是生产单质硅过程中的一个重要反应:SiO2+2C
Si+2CO↑,该反应的基本类型是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应难度: 中等查看答案及解析
-
如图所示,烧杯中盛有质量相等、质量分数相等的稀盐酸,天平调平后,同时向其中分别加入等质量的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
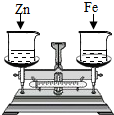
A.向左偏
B.向右偏
C.先向左偏后向右偏
D.先向右偏后向左难度: 中等查看答案及解析
-
甲、乙两种固体的溶解度曲线如右下图.将①②两试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里.升高温度后,下列有关说法正确的是( )

A.①②两溶液的质量一定相等
B.①②两溶液均变为不饱和溶液
C.①溶液质量增加,②溶液质量减少
D.①溶液中溶质的质量分数一定大于②溶液难度: 中等查看答案及解析
-
如图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )
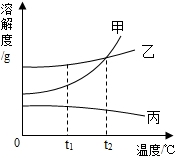
A.在t1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙
B.在t2℃时,甲、乙两物质的溶解度相等
C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙难度: 中等查看答案及解析
-
下列关于溶液的说法中,正确的是( )
A.当饱和溶液析出晶体后,剩余溶液中溶质的质量分数一定减少
B.某溶液降低温度后能析出晶体,则原溶液一定是饱和溶液
C.接近饱和的硝酸钾溶液,通过蒸发溶剂或加溶质的方法都可以达到饱和状态
D.20℃,氯化钠的溶解度为36g,则20℃时100g氯化钠饱和溶液中含有氯化钠36g难度: 中等查看答案及解析
-
如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是( )
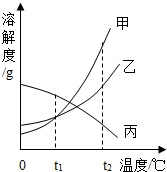
A.甲>乙>丙
B.甲=乙=丙
C.甲=乙>丙
D.丙>甲=乙难度: 中等查看答案及解析