-
我国古代典籍中有”银针验毒”的记载,“银针验毒”的反应原理之一是
4Ag+2H2S +O2=2X+2H2O。下列有关该反应的说法不正确的是
A. 反应属于氧化反应 B. X的化学式是Ag2S
C. 反应前后元素的种类不变 D. 反应前后所有元素的化合价都发生了变化
难度: 中等查看答案及解析
-
质量守恒定律揭示了化学反应中( )
A. 反应条件 B. 哪些物质是反应物
C. 哪些物质是生成物 D. 反应物和生成物的质量关系
难度: 中等查看答案及解析
-
在反应2CO+O2
2CO2中,各物质间的质量比为
A.2:1:2 B.56:32:88
C.28:32:44 D.1:1:2
难度: 简单查看答案及解析
-
“洁厕灵”与“漂白精”不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H2O,则X的化学式为
A. H2 B. ClO2 C. O2 D. Cl2
难度: 中等查看答案及解析
-
下列化学方程式书写正确的是( )
A. H2O2
H2O+O2↑ B. C+O2
CO2↑
C. 4P+5O2
2P2O5 D. 4Fe+3O2
2Fe2O3
难度: 中等查看答案及解析
-
下列关于化学方程式4P+5O2
2P2O5的读法,错误的是( )
A.磷和氧气在点燃的条件下反应生成五氧化二磷
B.在点燃的条件下,每4体积的磷和5体积的氧气完全反应,生成五氧化二磷
C.在点燃的条件下,每4个磷原子和5个氧气分子结合生成2个五氧化二磷分子
D.在点燃的条件下,每124份质量的磷和160份质量的氧气完全反应,生成284份质量的五氧化二磷
难度: 中等查看答案及解析
-
己知A+3B=2C+3D中,已知2.3gA跟4.8gB恰好完全反应生成4.4gC。又知D的相对分子质量为18,则A的相对分子质量为
A. 23 B. 46 C. 92 D. 96
难度: 中等查看答案及解析
-
下列关于化学反应2X+Y==2Z的叙述,错误的是( )
A. Z一定是化合物
B. 在反应中X、Y、Z三种物质的粒子数目比为2:1:2
C. 若X和Y的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
D. 若ag X完全反应生成bgZ,则同时消耗(b-a)gY.
难度: 中等查看答案及解析
-
化学变化中不能实现的变化是( )
A. 一种分子变成另一种分子 B. 一种离子变成另一种离子
C. 一种原子变成另一种原子 D. 一种单质变成另一种单质
难度: 中等查看答案及解析
-
下图表示某化学反应的微观示意图,依据图分析判断,下列说法正确的是
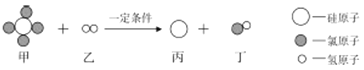
A. 甲物质由5个原子构成
B. 化学变化的后硅元素的化合价不变
C. 参加反应的乙的质量和生成的丁中氢元素的质量相等
D. 参加反应的甲、乙两种物质的分子个数比为l:1
难度: 中等查看答案及解析
-
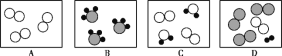
如图为两种物质间发生化学反应的微观示意图(一种小球代表一种原子)。下列说法中正确的是

A. 图示中共有三种单质分子
B. 图示产物为混合物
C. 图示说明在化学反应中分子不可再分
D. 图示化学反应属于化合反应
难度: 中等查看答案及解析
-
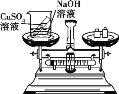
下图是某化学反应过程的微观示意图,下列有关说法正确的是

A. 反应前后分子的个数不变 B. 生成物有三种
C. 反应前后汞原子和氧原子的个数不变 D. 汞和氧气都由分子构成
难度: 中等查看答案及解析
-
三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是( )
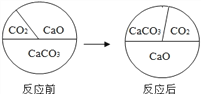
A. 反应中CaO为催化剂 B. 该反应是化合反应
C. 反应后容器中固体质量减少 D. 反应后容器中氧元素量分数增大
难度: 中等查看答案及解析
-
在化学反应2A+B2=2AB中,A 与B2反应的质量关系如图所示,现将6g A和8g B充分反应,则生成AB的质量是( )
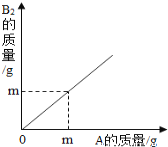
A. 9g B. 11g C. 12g D. 14g
难度: 中等查看答案及解析
-
某纯净物3g在氧气中完全燃烧,生成
二氧化碳和
水。下列说法不正确的是
A. 该纯净物中含有C、H元素,不含O元素
B. 该反应中
和
的质量比为14:11
C. 该反应中
和
的分子数之比为7:6
D. 该纯净物中C、H原子的个数比为1:4
难度: 中等查看答案及解析