-
下列语句中隐含化学变化的是
A.燃灶液化气化液灶燃 B.上海自来水来自海上
C.黄山落叶松叶落山黄 D.香山红叶寺叶红山香
难度: 简单查看答案及解析
-
分类是科学研究的重要方法,下列物质分类不正确的是
A.化合物:干冰,冰水混合物,烧碱,小苏打
B.非电解质:乙醇,四氯化碳,氯气,葡萄糖
C.同素异形体:活性炭,C60,C80,金刚石
D.混合物:漂白粉,纯净矿泉水,纯盐酸,石灰石
难度: 简单查看答案及解析
-
下列有关说法中,正确的是
A.从自然界中提取元素的单质都必须通过化学反应才能实现
B.碳酸钠可用于制备小苏打,治疗胃酸过多的药物,食品发酵剂
C.通过丁达尔效应可以鉴别稀豆浆和氢氧化铁胶体
D.焰火的五彩缤纷是某些金属元素的性质的展现
难度: 简单查看答案及解析
-
双羟基铝碳酸钠是医疗上常用的一种抑酸剂,其化学式为NaAl(OH)2CO3。关于该物质的说法正确的是
A.该物质属于两性氢氧化物
B.该物质是Al(OH)3和Na2CO3的混合物
C.1 mol NaAl(OH)2CO3最多可消耗3 mol H+
D.该药剂不适合于胃酸过多的胃病患者
难度: 中等查看答案及解析
-
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,明显不正确的是
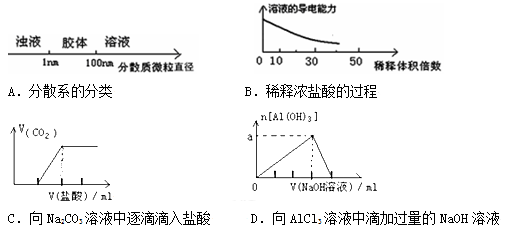
难度: 中等查看答案及解析
-
我们常用“往伤口上撒盐”来比喻某些人乘人之危的行为,其实从化学的角度来说,“往伤口上撒盐”的做法并无不妥,甚至可以说并不是害人而是救人。那么,这种做法的化学原理是
A.胶体的电泳 B.血液的氧化还原反应
C.血液中发生复分解反应 D.胶体的聚沉
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24 L CCl4中含Cl原子数目为0.4NA
B.白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA
C.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA
D.5.6g Fe和足量的盐酸反应时,失去的电子数为0.3NA
难度: 中等查看答案及解析
-
VL Fe2(SO4)3溶液中含有ag SO42-,取此溶液0.5VL,用水稀释至2VL,则稀释后溶液中Fe3+的物质的量的浓度为
A.
mol/L B.
mol/L
C.
mol/L D.
mol/L
难度: 中等查看答案及解析
-
将物质的量均为0.1 mol K2SO4和Al2(SO4)3溶于水,向其中加入一定量的Ba(OH)2溶液,测得铝元素有一半留在溶液中,则生成BaSO4的物质的量可能为
A.0.25 mol B.0.30 mol C.0.35 mol D.0.4 mol
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.100 mL 0.1 mol·L-1 Na2SO4溶液中,粒子总数是0.03NA
B.常温常压下,32 g O2-中所含电子的数目为17NA
C.1 mol Al3+完全水解生成氢氧化铝胶体粒子的数目为NA
D.标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定
难度: 中等查看答案及解析
-
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abc B.bcd C.abcd D.acd
难度: 中等查看答案及解析
-
日常生活中的下列现象与胶体的性质无关的是
A.将盐卤或石膏加入豆浆中制成豆腐
B.一枝钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
C.向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
D.清晨,阳光穿过树林枝叶间的间隙形成“光柱”
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.Na2O2投入水中:2Na2O2+2H2O = 4Na++4OH−+ H2↑
B.过量氯气通入溴化亚铁溶液中:2Cl2 +2Fe2+ +2Br-=4Cl-+2Fe3++ Br2
C.次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl—+H2O=Cl2↑+2OH—
D.NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O
难度: 中等查看答案及解析
-
限用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式:2H++SO32-=H2O+SO2↑的化学方程式个数有
A.4 B.5 C.8 D.12
难度: 简单查看答案及解析
-
下列各组离子中,能在同一溶液中大量共存,加入一小块钠后仍能大量共存的是
A.Na+、K+、Cl-、CO32- B.Cu2+、Na+、SO42-、NO3-
C.Ba2+、K+、Cl-、SO42- D.K+、Na+、HCO3-、CO32-
难度: 中等查看答案及解析
-
医院里用HgCl2的稀溶液作手术刀的消毒剂。HgCl2熔融时不导电,熔点低。HgS难溶于水和稀的强碱,却易溶于饱和的NaCl溶液。关于HgCl2的描述合理的是
A.是难溶的共价化合物
B.是一种强电解质
C.是离子化合物
D.是一种弱电解质
难度: 简单查看答案及解析
-
下列离子方程式的书写及评价均合理的是
选项
离子方程式
评价
A
将1 mol Cl2通入含1 mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2
正确;Cl2过量,可将Fe2+、I-均氧化
B
Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++HCO3-+OH-=MgCO3↓+H2O
正确;酸式盐与碱反应生成正盐和水
C
过量SO2通入NaClO溶液中:SO2+H2O+ClO-=HClO+HSO3-
正确;说明酸性:H2SO3强于HClO
D
1 mol·L-1的NaAlO2溶液和2.5 mol·L-1的HCl溶液等体积互相均匀混合:2AlO2-+5H++4H2O=Al3++Al(OH)3↓+5H2O
正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2∶3[
难度: 中等查看答案及解析
-
二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理常采用:2NaClO3 + 4HCl = 2ClO2↑+Cl2↑+2H2O+2NaCl,下列关于该反应的说法中正确的是
A.浓盐酸在反应中仅体现还原性
B.氧化性:NaClO3 <ClO2
C.每生成0.lmol ClO2转移0.5mol电子
D.被氧化和被还原的物质的物质的量之比为1:1
难度: 中等查看答案及解析
-
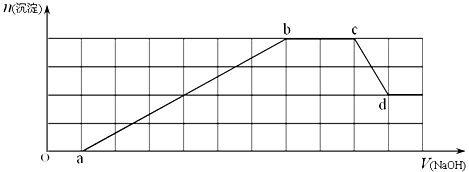
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL澄清溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则
A.反应过程中得到6.72L的气体(标准状况下)
B.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
C.最终得到7.8g的沉淀
D.最终得到的溶液中c(NaCl)=1.6 mol/L
难度: 中等查看答案及解析
-
下列各组物质相互混合,既有气体生成又有沉淀生成的是①金属钠投入到CuSO4溶液中②过量的NaOH溶液和明矾溶液 ③NaAlO2溶液和NaHCO3溶液混合 ④过量的Na2O2投入FeCl2溶液 ⑤金属钠投入NH4Cl溶液中
A.①④ B.②③ C.②③ D.①⑤
难度: 中等查看答案及解析