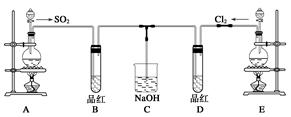
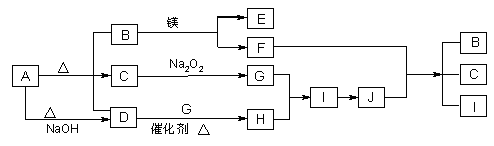
-
下列试剂能贮存在磨口玻璃塞的试剂瓶里的是( )
A.HF溶液 B.KOH溶液 C.盐酸 D.水玻璃
难度: 简单查看答案及解析
-
下图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法不正确的是( )
R
X
Y
Z
A.Y的氢化物比X的氢化物更稳定
B.原子半径大小顺序是Z>Y>X>R
C.Z的单质能与Y的某些化合物发生置换反应
D.X、Y、Z三种元素中,其最高价氧化物对应水化物的酸性强弱顺序是Z>Y>X
难度: 困难查看答案及解析
-
下列各组气体中,在通常情况下既能用浓硫酸又能用碱石灰干燥的有( )
A.CO、O2、N2 B.HCl、Cl2、CO2 C.NH3、H2、CO D.SO2、Cl2、O2
难度: 中等查看答案及解析
-
已知短周期元素的离子:aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径A>B>D>C B.原子序数d>c>b>a
C.离子半径C>D>B>A D.单质的还原性A>B>D>C
难度: 困难查看答案及解析
-
下图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶管的胶头,下列与实验事实不相符的是( )

A.CO2(NaHCO3溶液) 无色喷泉
B.NH3(H2O含酚酞)红色喷泉
C.SO2(NaOH溶液)无色喷泉
D.HCl(AgNO3溶液)白色浑浊喷泉
难度: 中等查看答案及解析
-
VL含有(NH4)2SO4、NH4NO3的混合溶液,加入a mol NaOH后,加热,恰好使NH3全部逸出;又加入b mol BaCl2则刚好使SO42-完全沉淀,则原混合溶液中NH4NO3的物质的量浓度为( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下图装置可用于( )

A.加热NaHCO3制CO2 B.用Cu与稀HNO3反应制NO
C.用NH4Cl与浓NaOH溶液反应制NH3 D.用KMnO4与浓HCl反应制Cl2
难度: 中等查看答案及解析
-
1999年1月,俄美科学家联合小组宣布合成出114号元素的一种同位素,该同位素原子的质量数为298。以下叙述不正确的是( )
A.该元素属于第七周期 B.该元素位于ⅢA族
C.该元素为金属元素,性质与82Pb相似 D.该同位素原子含有114个电子,184个中子
难度: 中等查看答案及解析
-
下列各组微粒具有相同的质子数和电子数的是( )
A.CH4、NH3、H2 B.OH-、F-、Ne
C.H3O+、NH4+、Na+ D.O2-、F-、Mg2+
难度: 中等查看答案及解析
-
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO2、N2O4的混合气体,这些气体与1.68LO2 (标准状况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入10mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗溶液NaOH的体积是( )
A.60
B.45
C. 30
D. 15
难度: 中等查看答案及解析
-
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是( )
A.单质的氧化性按X、Y、Z的顺序增强 B.阴离子的还原性按X、Y、Z的顺序减弱
C.气态氢化物的稳定性按X、Y、Z的顺序增强 D.元素非金属性按X、Y、Z的顺序减弱
难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.氯气溶于水中 Cl2 +H2O = Cl― + ClO― +2H+
B.金属铁与稀硝酸反应 Fe + 2H+ = Fe2+ + H2↑
C.在硅酸钠溶液中滴加稀硫酸 SiO32― + 2H+ = H2SO3↓
D.铜粉与98.3%的硫酸加热下反应 Cu + 4H+ + SO42― = Cu2+ + SO2↑ + 2H2O
难度: 简单查看答案及解析
-
我国最新报导的高超导体中,铊(Tl)是其中之一,已知位于第六周期第ⅢA族,关于铊的说法,可能错误的是:( )
A.Tl(OH)3 有两性 B.是银白色金属
C.与稀盐酸反应生成盐酸盐 D.铊的金属性强于铝的金属性
难度: 简单查看答案及解析
-
下列关于浓硝酸和浓硫酸的叙述错误的是( )
A.分别露置在空气中,容器内溶质的物质的量浓度都降低
B.都是常用的干燥剂
C.都可以储存于铝制槽罐中
D.和铜反应中都表现出强氧化性和酸性
难度: 简单查看答案及解析
-
短周期元素中,族序数等于周期数的两倍的两元素形成的化合物的化学式是( )
A.CS2 B.CO2 C.SO2 D.SiO2
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
难度: 中等查看答案及解析
-
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是.( )
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
难度: 困难查看答案及解析
-
稀硫酸中插一块铜片,加入下列物质后,可使铜片迅速发生反应的是( )
A.稀盐酸 B.硫酸钠晶体 C.硝酸钾晶体 D.氯化钠晶体
难度: 中等查看答案及解析
-
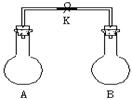
如图所示,室温下A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当打开止水夹K,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
编 号
①
②
③
A中气体
H2
NH3
NO
B中气体
Cl2
HCl
O2
A、 ②③① B、 ③①② C、③②① D、 ①②③
难度: 中等查看答案及解析
-
有三种金属元素a、b、c,在相同条件下,b的最高价氧化物的水化物的碱性比a的最高价氧化 物的水化物的碱性强;a可以从c的盐溶液中置换出c。则这三种金属元素的金属性由强到弱的顺序是( )
A.a、b、c B.b、a、c C.b、c、a D.c、b、a
难度: 中等查看答案及解析
-
X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
A.由mXa+与nYb-,得m+a=n-b
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
难度: 中等查看答案及解析
-
下列除杂的操作方法不正确的是 ( )
A.NO中有少量的NO2:用水洗涤后再干燥
B.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干
C.N2中有少量的O2:通过灼热的铜网
D.CO2中混有少量的SO2气体:通过饱和NaHCO3溶液洗气
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
难度: 中等查看答案及解析
-
物质的量之比为 2∶5 的锌与稀硝酸反应,若硝被还原的产物为 N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1:4 B.1:5 C.2:3 D.2:5
难度: 中等查看答案及解析
-
X元素原子的质量数为m,核内中子数为n,则Wg X2+ 离子含有的电子的物质的量约为( )
A. (m+n+2)w/m mol B. (m-n+2)w/m mol
C. (m+n-2)w/m mol D. (m-n-2)w/m mol
难度: 中等查看答案及解析