-
“富勒烯”家族又增添了新成员,继C60、C70、N60之后,中美科学家首次发现了全硼富勒烯B40。下列说法正确的是
A.B40和C70都属于新型化合物
B.C60和N60于同分异构体
C.B40、C60、N60、C70都只含共价键
D.B40、C60、N60、C70都属于烯烃
难度: 中等查看答案及解析
-
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项
现象或事实
解释
A
用浸有酸性高锰酸钾溶液的硅藻
土作水果保鲜剂
酸性高锰酸钾溶液能氧化水果释放的催熟剂乙烯
B
用氢氟酸蚀刻玻璃
Si02是碱性氧化物,能溶于酸
C
过氧化钠作呼吸面具中的供氧剂
过氧化钠是强氧化剂,能氧化二氧化碳
D
Al(OH)3用作塑料的阻燃剂
Al(OH)3受热熔化放出大量的热
难度: 中等查看答案及解析
-
W、X、Y、Z均是短周期元素,X、Y、Z处于同一周期,w、X、Z的简单离子具有相同的电子层结构,W的单质是空气中含量最多的气体,X的氧化物具有两性,Y的最高正价与最低负价的代数和为O,下列说法正确的是
A.单质熔点:w>Z B.离子半径:w>x>Z
C.最高正价:w>X>Z D.原子序数:Z>w>Y
难度: 中等查看答案及解析
-
近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu20+H2O=2Cu+2Li++20H-,下列说法不正确的是

A、放电时,Li+透过固体电解质向Cu极移动
B、放电时,负极的电极反应式为 Cu2O+H2O+2e-=Cu+2OH-
C、通空气时,铜被腐蚀,表面产生Cu20
D、整个反应过程中,铜相当于催化剂
难度: 中等查看答案及解析
-
下列实验操作对应的实验现象和解释或结论都正确的是
选项
实验操作
实验现象
解释或结论
A
把S02通人紫色石蕊试液中
紫色褪去
S02具有漂白性
B
向NaOH溶液中滴加足量的MgCl2溶液,
然后再滴加足量的CuCl2溶液
先产生白色沉淀,然
后沉淀变蓝色
C
向某溶液中滴加KSCN溶液
溶液变红色
溶液中含有Fe2+
D
将充满N02的密闭玻璃球浸泡在热水中
红棕色变深
反应2NO2⇋N2O4的△H<0
难度: 中等查看答案及解析
-
向某恒容密闭容器中充入一定量C02和H2:,发生反应:

测得平衡体系中C02的百分含量(CO2%)与反应温度变化的关系如图所示。下列物理量中,a点大于b点的是
①正反应速率②逆反应速率③HCOOH(g)的浓度④对应温度时的平衡常数

A.①② B.①③ C.②④ D.③④
难度: 中等查看答案及解析
-
常温下,下列有关醋酸的叙述中不正确的是
A.pH=5.6的由CH3COOH与CH3COONa组成的混合溶液中: c(Na+)<c(CH3C00-)
B.将PH=a的醋酸稀释为pH=a+1的过程中,C(OH-)不断增大
C.等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14
D.浓度均为0.1 mol·L-1的CH3COOH溶液和氨水等体积混合后:

难度: 中等查看答案及解析
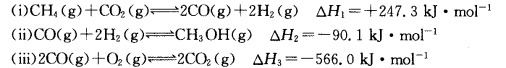
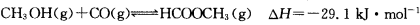 ,科研人员对该反应进行了研究,部分研究结果如下:
,科研人员对该反应进行了研究,部分研究结果如下: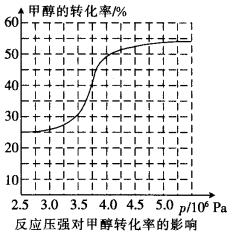
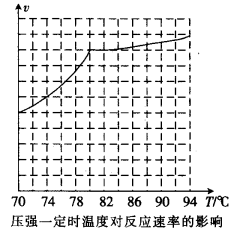
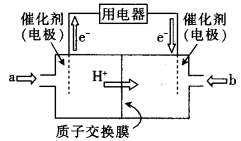
 )
)