-
下列有关实验操作、现象和解释或结论都正确的是 ( )
选项
实验操作
现象
解释或结论
A
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液
溶液呈红色
稀HNO3将Fe氧化为Fe3+
B
常温下,Fe、Al放入浓HNO3或浓H2SO4中
无明显现象
Fe、Al与浓HNO3或浓H2SO4发生钝化
C
Al箔插入稀HNO3中
无现象
Al箔表面被HNO3氧化,形成致密的氧化膜
D
用玻璃棒蘸取浓HNO3点到红色石蕊试纸上
试纸变蓝色
浓HNO3具有酸性
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A. Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂
B. ClO2具有还原性,可用于自来水的杀菌消毒
C. SiO2硬度大,可用于制造光导纤维
D. NH3易溶于水,可用作制冷剂
难度: 中等查看答案及解析
-
同一周期X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性是: HXO4>H2YO4>H3ZO4,则下列判断错误的是
A. 原子半径:X > Y > Z B. 气态氢化物的稳定性:HX > H2Y > ZH3
C. 非金属性:X > Y > Z D. 阴离子的还原性:Z3-> Y2-> X-
难度: 中等查看答案及解析
-
a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和C+离子的电子层结构相同,d与b同族。下列叙述错误的是()
A. a与其他三种元素形成的二元化合物中其化合价均为+1
B. b与其他三种元素均可形成至少两种二元化合物
C. c的原子半径是这些元素中最大的
D. d和a形成的化合物的溶液呈弱酸性
难度: 中等查看答案及解析
-
中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于
的叙述错误的是
A. 原子序数116 B. 中子数177
C. 核外电子数116 D. 相对原子质量293
难度: 中等查看答案及解析
-
与OH- 具有相同质子数和电子数的微粒是( )
A. NH3 B. HF C. NH4+ D. F-
难度: 简单查看答案及解析
-
下列递变规律不正确的是( )
A. Na、Mg、Al的还原性依次减弱 B. I2、Br2、Cl2的氧化性依次增强
C. C、N、O的原子半径依次增大 D. P、S、Cl的最高正化合价依次升高
难度: 中等查看答案及解析
-
下列有关性质的比较,不能用元素周期律解释的是
A. 酸性:H2SO4>H3PO4 B. 非金属性:Cl>Br
C. 碱性:NaOH>Mg(OH)2 D. 热稳定性:Na2CO3>NaHCO3
难度: 中等查看答案及解析
-
下列关于原子结构、元素性质的说法正确的是
A. 非金属元素组成的化合物中只含共价键
B. IA族金属元素是同周期中金属性最强的元素
C. 同种元素的原子均有相同性质的质子数和中子数
D. VIIA族元素的阴离子性还原性越强,其最高价氧化物对应水化物的酸性越强
难度: 中等查看答案及解析
-
下列关于氨水的叙述正确的是
A. 氨水显碱性,是因为氨水是一种弱碱
B. 氨水和液氨成分相同
C. 氨水中物质的量浓度最大的粒子是NH3·H2O(除水外)
D. 氨水中共有五种粒子
难度: 简单查看答案及解析
-
在给定条件下,下列选项所示的物质间转化均能实现的是
A. Fe
FeCl2
Fe(OH)2
B. S
SO3
H2SO4
C. CaCO3
CaO
CaSiO3
D. NH3
NO
HNO3
难度: 困难查看答案及解析
-
如图为元素周期表截取的短周期的一部分,四种元素均不是稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是 ( )
A. 原子半径:W>Z>Y>X
B. 气态氢化物的稳定性:Z>W>X>Y
C. W的最高正化合价与负化合价的绝对值一定不相等
D. Z的最高价氧化物的水化物可能为弱酸
难度: 中等查看答案及解析
-
下列化学反应的离子方程式正确的是( )
A. 用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑
B. 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO
C. 在稀氨水中通入过量CO2:NH3·H2O+CO2===NH4++HCO3-
D. 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-===CaSO4↓+H2O
难度: 简单查看答案及解析
-
某同学在实验室中发现了一瓶无色、有刺激性气味的气体,根据气味判断可能是氨气,但不能确定一定是氨气。下列提供的方法中,你认为能够帮他检验是否为氨气的是
A. 将湿润的红色石蕊试纸放在打开的瓶口
B. 将湿润的蓝色石蕊试纸放在打开的瓶口
C. 用蘸有浓硫酸的玻璃棒靠近打开的瓶口
D. 用干燥的红色石蕊试纸放在打开的瓶口
难度: 中等查看答案及解析
-
下列关于浓硫酸的叙述正确的是( )
A. 浓硫酸具有吸水性,因而能使蔗糖碳化
B. 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C. 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D. 浓硫酸在常温下能够使铁、铝等金属钝化
难度: 简单查看答案及解析
-
下列反应中硝酸既能表现出酸性又表现出氧化性的是( )
A. 使石蕊试液变红
B. 与铜反应放出NO气体,生成Cu(NO3)2
C. 与Na2CO3反应放出CO2气体,生成NaNO3
D. 与S单质混合共热时生成H2SO4和NO2
难度: 中等查看答案及解析
-
下列有关铜与浓硝酸反应的说法中错误的是
A. HNO3是氧化剂,NO2是还原产物
B. 若2 mol HNO3被还原,则反应中一定生成22.4 L NO2气体
C. 参加反应的硝酸中,被还原和未被还原的硝酸的物质的量之比是1∶1
D. 硝酸在反应中既表现了强氧化性,又表现了酸性
难度: 困难查看答案及解析
-
如图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液。挤压胶管的胶头,下列与实验事实不相符的是 ( )

A. NH3(H2O含石蕊) 蓝色喷泉 B. HCl (H2O含石蕊) 红色喷泉
C. C12(饱和食盐水) 无色喷泉 D. CO2(NaOH溶液) 无色喷泉
难度: 中等查看答案及解析
-
为检验一种氮肥的成分,某学习小组的同学进行了以下实验:
①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。
②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。
由此可知该氮肥的主要成分是
A. NH4HCO3 B. NH4Cl
C. (NH4)2CO3 D. NH4NO3
难度: 中等查看答案及解析
-
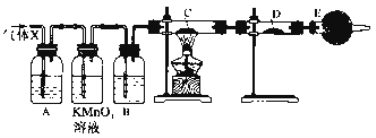
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是

①洗气瓶中产生的沉淀中有碳酸钡
②在Z导管出来的气体中无二氧化碳
③洗气瓶中产生的沉淀是硫酸钡
④在Z导管口有红棕色气体出现
A. ①② B. ③④ C. ①④ D. ②③
难度: 困难查看答案及解析
-
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是
A. 元素的非金属性次序为c>b>a
B. a和其他3种元素均能形成共价化合物
C. d和其他3种元素均能形成离子化合物
D. 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
难度: 困难查看答案及解析
-
Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍。下列说法正确的是 ( )

A. 原子半径大小顺序为r(Q)>r(R)>r(T)>r(M)>r(W)
B. Q、W的单核离子的核外电子数相等
C. 五种元素均能形成氢化物
D. W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强
难度: 中等查看答案及解析
-
在某100 mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L−1、0.2 mol·L−1。向该混合液中加入1.92 g铜粉,加热,待充分反应后(假设反应前后溶液体积不变),所得溶液中的Cu2+的物质的量浓度(mol·L−1)是( )
A. 0.15 B. 0.225 C. 0.3 D. 0.45
难度: 中等查看答案及解析
-
科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IVA族,称为类铅。关于它的性质,预测错误的是
A. 它的最外层电子数为4 B. 它的金属性比铅强
C. 它具有+2、+4价 D. 它的最高价氧化物的水化物是强酸
难度: 困难查看答案及解析