-
下列与化学反应能量变化相关的叙述正确的是
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同
压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
难度: 中等查看答案及解析
-
下列反应既是氧化还原反应,又是吸热反应的是
A.灼热的炭与CO2反应 B.铝片与稀H2SO4反应
C.Ba(OH)2·8H2O与NH4Cl的反应 D.甲烷在O2中的燃烧反应
难度: 简单查看答案及解析
-
根据热化学方程式:S(g)+O2(g)=SO2(g)ΔH=-QkJ·mol-1(
Q>0),则下列分析正确的是
A.1molS(g)与1molO2(g)的总能量比1molSO2(g)的总能量低QkJ
B.1molS(g)与1molO2(g)反应生成1molSO2(g)放出QkJ的能量
C.S(s)+O2(g)=SO2(g)ΔH<-QkJ·mol-1
D.1个S(g)与1个O2(g)完全反应可放出QkJ的能量
难度: 中等查看答案及解析
-
下列有关热化学方程式的叙述正确的是
A.已知甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g)=2CO2(g)+2H2O(g)ΔH=-890.3kJ·mol-1
B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定
C.已知中和热为ΔH=-57.4kJ·mol-1,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热
D.CO(g)的燃烧热是283.0kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+(2×283.0)kJ·mol-1
难度: 中等查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-l;
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220kJ·mol-l.
现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3847 kJ,则在混合气体中H2和C3H8的体积比是( )
A.2:1 B.3:1 C.4:1 D.5:1
难度: 困难查看答案及解析
-
在298K、100kPa时,已知:
2H2O(g)=O2(g)+2H2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3
,
则△H3与△H1和△H2间的关系正确的是
A.△H3=△H1+2△H2 B.△H3=△H1+△H2 C.△H3=△H1-2△H2 D.△H3=△H1-△H2
难度: 困难查看答案及解析
-
已知化学反应A2(g)+B2(g)=2AB(g) ΔH=Q kJ·mol-1,其能量变化如图所示,则Q的值正确的是
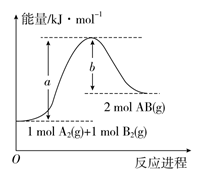
A.a-b
B.a
C.-b
D.b-a
难度: 中等查看答案及解析
-
通常人们把拆开1 mol某化学键所吸收的能量或形成1 m
ol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
化学健
H-H
Cl-Cl
H-Cl
键能
436 kJ/mol
243 kJ/mol
431 kJ/mol
则下列热化学方程式不正确的是
A.1/2 H2(g)+1/2Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g) ΔH=-183 kJ·mol-1
C.2HCl(g)=H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
D.1/2 H2(g)+1/2Cl2(g)=HCl(g) ΔH=+91.5 kJ·mol-1
难度: 困难查看答案及解析
-
在密闭容器里,A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示,已知3v(B)=2v(A)、2v(C)=3v(B),则此反应可
表示为
A.2A+3B = 2C B.A+3B = 2C C.3A+2B = 3C D.A+B = C
难度: 中等查看答案及解析
-
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是
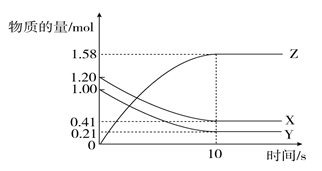
A.反应开始到10 s,用Z表示的反应速率为0.158 mol·(L·s)-
1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)=Z(g)
难度: 困难查看答案及解析
-
在C(s)+CO2(g)
2CO(g)的反应中,现采取下列措施:①缩小体积 ②增加碳的量 ③通入CO2④恒容下充入He ⑤恒压下充入He ⑥加热,其中能够使反应速率增大的措施是
A. ①④ B.②③⑤ C. ①③⑥ D.①②④
难度: 中等查看答案及解析
-
对于反应A(g)+3B(g)⇌2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.01 mol/(L•s) B.v(B)=0.02 mol/(L•s)
C.v(B)=0.60mol/(L•min) D.v(C)=1.0mol/(L•min)
难度: 中等查看答案及解析
-
下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增加
B.对于有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大
C.改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率
D.对于本来不能发生的化学反应,改变条件可以使反应发生
难度: 中等查看答案及解析
-
在容积为1L的密闭容器中,充入1mol CO2和3mol H2,在温度500℃时发生反应:CO2(g)+ 3H2(g)
CH3OH(g)+ H2O(g) △H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是

A.从反应开始到10分钟时,H2的平均反应速率v(H2)=0.15 mol/(L·min)
B.
从20分钟到25分钟达到新的平衡,可能是增大压强
C.其它条件不变,将温度升到800℃,再次达平衡时平衡常数减小
D.从开始到25分钟,CO2的转化率是70%
难度: 困难查看答案及解析
-
在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g)
C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是
①混合气体的密度 ②混合气体的压强 ③B的物质的量浓度 ④混合气体的总物质的量
A.①② B.②③ C.①③
D.①④
难度: 中等查看答案及解析
-
在一定条件下,红棕色的NO2可以发生如下反应:2NO2(g)
2NO(g)+O2(g) △H>0,下列叙述中正确的是
A.恒温恒容,充入NO2气体,其转化率增大
B.加压,平衡向逆反应方向移动,混合气体颜色变深
C.若平衡常数增大,则可能是升高了温度或减小了体系的压强
D.当2v正(NO)=v逆(O2)时,反应达到化学平衡状态
难度: 中等查看答案及解析
-
对于可逆反应:2A(g)+B(g)⇌2C(g);△H<0,下列各图正确的是(设变化过程中物质的聚集状态没有发生改变)

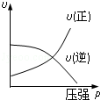
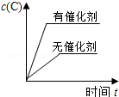

A B C D
难度: 困难查看答案及解析
-
下列关于焓判据和熵判据的说法中,不正确的是
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.由焓判据和熵判据组合成的复合判据,将更适合于所有的过程
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200 K)下则能自发进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
难度: 中等查看答案及解析
-
H2S水溶液中存在电离平衡H2S
H++HS-和HS-
H++S2-,若向H2S溶液中
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH增大
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
难度: 中等查看答案及解析
-
在100 mL 0.1 mol·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是
A.加热 B.加入100 mL 0.1 mol·L-1的醋酸溶液
C.加入少量的0.5 mol·L-1的硫酸 D.加入少量的1 mol·L-1的NaOH溶液
难度: 中等查看答案及解析
-
在25℃时,0.1 mol·L-1的HNO2、HCOOH、HCN、H2CO3的溶液中,它们的电离平衡常数分别为4.6×10-4、1.8×10-4、4.9×10-10、K1=4.3×10-7和K2=5.6×10-11,其中氢离子浓度最小的是
A.HNO2 B.HCOOH C.HCN D.H2CO3
难度: 中等查看答案及解析