-
2004年2月22日是第35个“世界地球日”,我国确定的主题是“善待地球--科学发展”.下列行为中不符合这一主题的是( )
A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.大量开采地下水,以满足社会对水的需求
C.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
D.节约能源,提高能源利用率难度: 中等查看答案及解析
-
下列各组微粒中,核外电子总数相等的是( )
A.Na+和K+
B.NO和NO2
C.H2O 和Mg2+
D.NO和CO难度: 中等查看答案及解析
-
在下列反应中,属于氧化还原反应的是( )
A.2H2O22H2O+O2
B.CaCO3CaO+CO2
C.CaO+H2O=Ca(OH)2
D.CaCO3+2HCl=CaCl2+CO2↑+H2O难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.28g氮气所含有的原子数目为NA
B.化学反应中1mol金属镁变成镁离子时失去电子数目为2NA
C.标准状况下,22.4L水中含有NA个水分子
D.标准状况下,22.4L氯化氢所含的原子数为NA难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.1 molH2O的质量是18 g•mol-1
B.CO2的摩尔质量为44 g
C.NaOH的相对分子质量是40 mol-1
D.H的摩尔质量是1 g•mol-1难度: 中等查看答案及解析
-
进行焰色反应实验时,通常用来洗涤铂丝的是( )
A.硫酸
B.烧碱溶液
C.稀盐酸
D.蒸馏水难度: 中等查看答案及解析
-
浊液区别于其他分散系最本质的特征是( )
A.外观浑浊不清
B.浊液没有丁达尔现象
C.不稳定
D.分散质粒子直径大于100nm难度: 中等查看答案及解析
-
下列各组物质中,不符合前者为混合物,后者为单质的是( )
A.Na2CO3•10H2O Na2CO3
B.氯水 液氮
C.石油 液氢
D.碘酒 氦难度: 中等查看答案及解析
-
下列实验操作中,不能用于物质分离的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
漂白粉的有效成分是( )
A.次氯酸钙
B.氯化钙
C.次氯酸
D.次氯酸钙与氯化钙难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大难度: 中等查看答案及解析
-
下列关于氯水的叙述正确的是( )
A.新制氯水中只含Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡放出,该气体主要是Cl2
D.氯水放置数天后pH值将变大难度: 中等查看答案及解析
-
23He可以作为核聚变材料.下列关于23He的叙述正确的是( )
A.23He和13He互为同位素
B.23He原子核内中子数为2
C.23He原子核外电子数为2
D.23He代表原子核内有2个质子和3个中子的氦原子难度: 中等查看答案及解析
-
以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有大量的SO42-
B.加入足量的CaCl2溶液,产生了白色沉淀.溶液中一定含有大量的CO32-
C.加入足量浓 NaOH溶液,产生了带有强烈刺激性气味,并能使湿润的红色石蕊试纸变蓝的气体.溶液中一定含有大量的NH4+
D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀.溶液中一定含有大量的Cl-难度: 中等查看答案及解析
-
下列图示实验操作中,正确的是( )
A.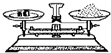
称取氢氧化钠
B.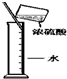
浓硫酸稀释
C.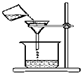
过滤溶液
D.
点燃酒精灯难度: 中等查看答案及解析
-
下列说法正确的是( )
A.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
B.稀释浓硫酸时,将水缓缓倒入盛浓硫酸的烧杯中,并用玻璃棒不断搅拌
C.用汽油萃取碘水中的碘单质的操作,可选用分液漏斗,而后静置分液
D.鉴别氯化铁溶液与氢氧化铁胶体较简便的方法是用激光束照射难度: 中等查看答案及解析
-
同温同压下,等质量的CO和CO2相比较,下列叙述中正确的是( )
A.体积比为1:1
B.体积比为11:7
C.原子数比为2:3
D.密度比为11:7难度: 中等查看答案及解析
-
下列实验操作一定要用到烧杯和玻璃棒的是( )
①过滤 ②萃取 ③溶解 ④向容量瓶转移液体 ⑤加热.
A.①②③
B.②③④
C.①③④
D.①②⑤难度: 中等查看答案及解析