-
下列说法不正确的是
A.08年北京奥运会开幕式上的“脚印”等焰火让全世界为之欢呼、倾倒,这主要是利用了化学中“焰色反应”的知识
B.我国神七宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C.中国第1艘LNG船“大鹏昊”已于09年5月2日满载65000吨LNG,抵达广东。船底镶嵌锌块,锌作负极,以防船体被腐蚀
D.2008年诺贝尔化学奖被授予研究“绿色荧光蛋白质”的美籍华裔科学家钱永健等人。蛋白质都是由氨基酸形成的不可降解的高分子化合物,其水溶液有丁达尔效应
难度: 简单查看答案及解析
-
下列叙述正确的是
①硫酸钡难溶于水和酸,可做X光透视肠胃的药剂
②蛋白质遇酒精会变性,医疗中用75%的乙醇溶液进行消毒
③棉花、蚕丝、人造羊毛的主要成分都是纤维素
④加酶洗衣粉是在洗衣粉中加入能使蛋白质水解的碱性蛋白酶,为了提高它的活性,洗衣服时温度越高效果越好
⑤碳酸钠、氢氧化钠、碳酸钙、碳酸氢钠等都可以中和酸,故都可以作为治疗胃酸过多的药物
⑥明矾净水利用了胶体的性质
⑦氢氟酸储存在玻璃瓶中
⑧可以用二氧化硅和水反应制备硅酸胶体
A.①②③⑦ B.①②⑥ C.①③④⑧ D.全都正确
难度: 简单查看答案及解析
-
室温时,柠檬水溶液的pH是3,其中的c(OH-)是
A.0.1 mol/L B.1×10-3 mol/L
C.1×10-7 mol/L D.1×10-11 mol/L
难度: 简单查看答案及解析
-
下列化学用语正确的是
A. 硫的原子结构示意图:
B.NH4Cl的电子式:
C.原子核内有8个中子的氧原子:
D.Be2+离子中的质子数和电子数之比为2:1
难度: 简单查看答案及解析
-
非金属氧化物采用不同的分类方法可分为不同的类别,从某种意义将N2O5、SO3、CO2、Cl2O7等归为一类。则下列氧化物与它们属于同一类的是
A.CO B.NO2 C.SO2 D. NO
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A. 用氯气作为水的消毒剂: Cl2+H2O = 2H++Cl-+ClO-
B. 用食醋清除热水瓶胆里的水垢:2H++CaCO3=Ca2++H2O+CO2↑
C. 胃药里含氢氧化铝能降低胃酸:Al(OH)3+3H+=Al3++3H2O
D.工业制烧碱: 2Cl-+ 2H2O = Cl2↑ +H2↑ + 2OH-
难度: 简单查看答案及解析
-
20世纪80年代人们发现和证实了碳的另一类单质,它们是一系列由偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个
C60连接而成的物质X,下列有关说法不正确的是

A.X难溶于水
B.X是高分子化合物
C.一定条件下X可与H2发生加成反应
D.X的摩尔质量为720n克/摩尔
难度: 简单查看答案及解析
-
下图各容器中盛有海水,铁在其中被腐蚀的速率由快到慢的顺序是
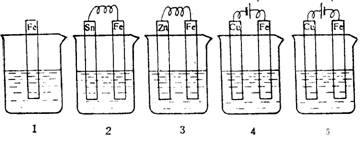
A.4>2>1>3>5 B.2>1>5>3>4C.5>2>1>3>4 D.4>3>1>2>5
难度: 简单查看答案及解析
-
下列方程式中,属于水解反应的是( )
A.H2O + H2O
H3O+ + OH—
B.HCO3— + OH— = H2O + CO32—
C.CO2 + H2O
H2CO3
D.CO32— + H2O
HCO3— + OH—
难度: 简单查看答案及解析
-
在指定的溶液中一定可以大量共存的离子组是
A.使石蕊变红的溶液中: Na+、I-、Cl-、NO3-、C6H5O-
B.在强碱性溶液中:Na+、K+、AlO2-、CO32-、SiO32-
C.在无色透明溶液中:NH4+、Fe3+、SO32-、NO3-
D.由水电离出来的c(H+) = 1×10-13 mol/L的溶液中:K+、CO32-、Cl-、NO3-
难度: 简单查看答案及解析
-
氯气是一种重要的化工原料。工业上利用反应:3Cl2 + 2NH3 = N2 + 6HCl检查氯气管道是否漏气。下列说法错误的是
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.生成1 mol N2有6 mol电子转移
D.该反应属于复分解反应
难度: 简单查看答案及解析
-
下列说法正确的是
A.7.1 g C12与足量NaOH溶液反应转移0.2×6.02×1023个电子
B.28 g乙烯和丙烯的混合气体中含有2×6.02×1023个碳原子
C.标准状况下,2.24 L H2O含有的分子数等于0.1 NA
D.2.9 g乙基(一C2H5)含有的电子数为1.8 NA个
难度: 简单查看答案及解析
-
有关下图所示化合物的说法不正确的是

A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
难度: 简单查看答案及解析
-
被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰。在纸内是离子“流过”水和氧化锌组成的电解液。电池总反应为:Zn + 2 MnO2十H2O = ZnO + 2MnO (OH)。下列说法正确的是
A.该电池的正极为锌
B.电池正极反应式为: 2MnO2 + 2e-+ 2H2O = 2MnO (OH)十2OH-
C.当 0.l mol Zn 完全溶解时,流经电解液的电子个数为 1.204×l023
D.该电池反应中二氧化锰起催化作用
难度: 简单查看答案及解析
-
为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是
A.KI(淀粉溶液) B.FeCl2溶液(KSCN)
C.Na2SO3溶液(BaCl2) D.HCHO溶液(石蕊试液)
难度: 简单查看答案及解析
-
X、Y、Z、W为四种短周期主族元素。其中X、Z同主族,Y、Z同周期,W与X、
Y既不同主族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正
价与最低负价的代数和为6。下列说法正确的是
A.X与W可以形成W2X、W2X2两种化合物
B.Y元素最高价氧化物对应水化物的化学式为H2YO4
C.Z的氢化物的沸点比X的氢化物的沸点高
D.Y、Z两元素的简单离子的半径Y>Z
难度: 简单查看答案及解析
-
MOH强碱溶液和等体积、等浓度的HA弱酸溶液混合后,溶液中有关离子的浓度应满足的关系是
A.c(M+)>c(OH-)>c(A-)>c(H+)
B.c(M+)> c(A-) > c(H+)> c(OH-)
C.c(M+)> c(A-) > c(OH-) >c(H+)
D.c(M+)> c(H+) >c(A-)> c(OH-)
难度: 简单查看答案及解析
-
以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加
过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在
内的沉淀,再经蒸发、结晶,可得纯净的MnCl2 ,根据上述实验事实可推知MnS具
有的相关性质是
A.具有吸附性
B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS
D.溶解度小于CuS、PbS、CdS
难度: 简单查看答案及解析
-
已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) === 2CO2(g)+2H2O(l) △H1= -870.3 kJ·mol-1
(2)C(s)+O2(g) === CO2(g) △H2= -393.5 kJ·mol-1
(3)H2(g)+O2(g) === H2O(l) △H3= -285.8 kJ·mol-1
则反应2C(s)+2H2(g)+O2(g)===CH3COOH(l) 的焓变△H为( )kJ·mol-1
A.488.3 B.-244.15 C.244.15 D.-488.3
难度: 简单查看答案及解析
-
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与2.24 L O2(标准状况)混合后通入水中,气体恰好完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入100 mL NaOH溶液,此时Cu2+恰好沉淀完全,所用NaOH溶液的浓度是( )mol·L-1
A.1 B.2 C.3 D.4
难度: 简单查看答案及解析
-
在一定温度下,反应
的平衡常数为9。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于
A. 10% B.18% C.20% D.40%
难度: 简单查看答案及解析