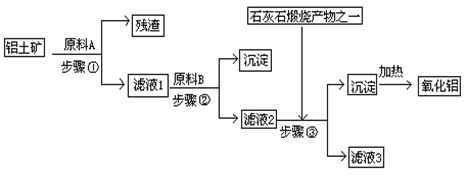
-
有15gA物质和10.5gB物质完全反应后,生成7.2gC物质,1.8gD物质和0.3molE物质,则E的摩尔质量是()
A. 100g/mol B. 111g/mol C. 55g/mol D. 27.5g/mol
难度: 简单查看答案及解析
-
化学是以实验为基础的自然科学,化学实验设计和操作中必须十分重视师生安全问题和环境保护问题。下列实验问题处理方法不正确的是( )
A.制氧气时用排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
B.在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷气体的纯度
C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
D.给试管中的液体加热时不时移动试管或加入碎瓷片,以免暴沸伤人
难度: 简单查看答案及解析
-
1个氧原子的质量是2.657×10-26kg,则32kgO2中所含O2的数目最接近于()
A. 3.01×1026 B. 5.32×1026 C. 6.02×1026 D. 1.2×1026
难度: 简单查看答案及解析
-
下列说法正确的是()
A.复分解反应中有的是氧化还原反应,有的不是氧化还原反应
B.置换反应有可能是非氧化还原反应
C.化合反应一定是氧化还原反应
D.分解反应不一定是氧化还原反应
难度: 简单查看答案及解析
-
下列各组物质中,一定都属于纯净物的是
A.液氯和氯水 B.酒精溶液和乙醇
C.饱和食盐水和硫酸亚铁 D.干冰和混有冰的水
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.1mol任何物质在标准状况下的体积都约是22.4L
B.0.5 mol氢气的体积为11.2L
C.在标准状况下,各为1mol的二氧化硫、三氧化硫的体积均约为22.4L
D.在20L恒容密闭容器中,充入1mol的氮气和3mol氢气,达平衡后有0.5mol的氮气反应,平衡后混合气体的体积仍为20L
难度: 简单查看答案及解析
-
下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②pH试纸的使用 ③过滤 ④蒸发
A. 试管 B. 胶头滴管 C. 玻璃棒 D. 漏斗
难度: 简单查看答案及解析
-
下列实验中所选用的仪器或操作合理的是( )
A.用托盘天平称量5.85 g氯化钠晶体
B.用湿润pH试纸测定某H2SO4溶液的pH
C.可用酸式滴定管量取25.00 mL高锰酸钾溶液
D.用瓷坩埚灼烧碳酸钠晶体
难度: 简单查看答案及解析
-
下列反应中,属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
A.SO2+H2O=H2SO3 B.Cl2+H2O=HCl+HClO
C.3Fe+4H2O(g)=Fe3O4+H2↑ D.2Na+2H2O=2NaOH+H2↑
难度: 简单查看答案及解析
-
用10mL0.1mol·L-1BaCl2溶液恰好可使同体积的Fe2(SO4)3、ZnSO4和K2SO4三种溶液中的SO42-完全转化为BaSO4沉淀,则三种溶液的物质的量浓度之比是( )
A.3︰2︰2 B.1︰2︰3 C.1︰3︰3 D.3︰1︰1
难度: 简单查看答案及解析
-
为了实现我国政府在1997年12月31日前对淮河流域环境的治理,某甲、乙两相邻的工厂做了横向联合.已知两厂排放的污水经初步处理后,只溶有Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-中的各不同的4种离子(设各离子浓度比较大),若单独排放仍会造成环境污染,如将两厂的污水按适当的比例混合,沉淀后污水变成无色澄清的硝酸钠溶液排出,则污染程度会大为降低.你认为下列分析判断正确的是 ( )
A.SO42- 和NO3-可存在于同一工厂 B.Cl-和NO3-一定在不同的工厂
C.Ag+和Na+可能在同一工 D.Na+和NO3-来自同一工厂
难度: 简单查看答案及解析
-
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2
LiNH2+LiH,下列有关说法正确的是
A. Li2NH中N的化合价是
B.该反应中H2既是氧化剂又是还原剂
C.
和
的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
难度: 简单查看答案及解析
-
除去NaCl中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④HCl。加入试剂合理的操作顺序是( )
A.①②③④ B.③①②④ C.④②①③ D.③②①④
难度: 简单查看答案及解析
-
某同学为证明NaOH溶液能使酚酞试液变红是OH-的性质,他所设计的下列实验中没有意义的是
A.取KOH、Ba(OH)2、Ca(OH)2溶液分别与酚酞试液作用,观察溶液颜色
B.取NaCl溶液与酚酞试液作用,观察溶液颜色
C.测定NaOH的溶解度,证明其易溶于水,并观察溶液的颜色
D.向滴有酚酞的NaOH溶液中加入盐酸,观察溶液的颜色
难度: 简单查看答案及解析
-
将钠和碳分别置于右图所示的两个盛满氧气的集气瓶中燃烧完毕后,打开装置中的两个活塞,这时观察到( )
、
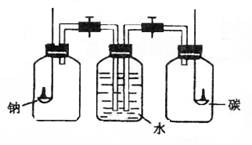
A.水进入右瓶 B.水进入左瓶
C.水同时进入两瓶 D.水不进入任何一瓶
难度: 简单查看答案及解析
-
设
为阿伏加德罗常数的数值,下列说法正确的是
A.16g
中含有4
个C-H键
B.1mol·
溶液含有
个
C.1mol Cu和足量稀硝酸反应产生
个NO分子
D.常温常压下,22.4L
中含有
个
分子
难度: 简单查看答案及解析
-
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH
、Ba2+、Cl-、CO
、SO
。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g。根据上述实验,以下推测正确的是
A.一定不存在Ba2+,NH
可能存在 B.CO
一定不存在
C.Na+一定存在 D.一定不存在Cl-
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.相同物质的量的任何物质具有相同数目的微粒
B.同物质的量浓度同体积的任何溶液中所含溶质微粒数目相同
C.含58.5 克氯化钠的溶液中含有6.02×1023个氯化钠分子
D.无论什么状况下,一定质量的某种气体含有的分子数是一定的
难度: 简单查看答案及解析
-
完全中和100mL0.1mol·L-1NaOH溶液,需要( )
A、100mL0.1mol·L-1H2SO4溶液 B、100mL0.1mol·L-1CH3COOH溶液
C、50mL0.1mol·L-1MgCl2溶液 D、100mLpH=1CH3COOH溶液
难度: 简单查看答案及解析
-
将15 mL 2 mol·L-1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1 MCln盐溶液中,恰好将溶液中的Mn+完全沉淀为碳酸盐,则MCln中n值是( )
A.4 B.3 C.2 D.1
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A.KOH的摩尔质量是56 g
B.一个碳原子的质量就是其相对原子质量
C.硫原子的质量就是硫的相对原子质量
D.氦气的摩尔质量(单位:g·mol-1)在数值上等于它的相对原子质量
难度: 简单查看答案及解析
-
下列有关化学方程式或离子方程式书写错误的是( )
A.将分别蘸有浓盐酸和浓氨水的玻璃棒靠近:NH3+HCl=NH4Cl
B.在酸性溶液中S2-和SO32 -不能共存:2S2-+SO32 -+6H+=3S↓+3H2O
C.不能用排空气法收集NO气体的原因:2NO+O2=2NO2
D.泡沫灭火器的工作原理:3CO32 -+2Al3++3H2O=2Al(OH)3↓+3CO2↑
难度: 简单查看答案及解析