-
如图,已知有以下物质相互转化
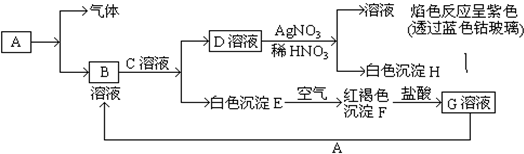
(1) A转化为B及气体这步反应中应加入的试剂是(填化学式) ,C溶液中溶质的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出检验G溶液中阳离子的离子方程式 ;向G溶液中加入A的有关离子反应方程式是 。
(4) 有一瓶存放时间较长的B溶液,某学生怀疑其有部分因氧化而变质,如果有变质,应如何除去变质的杂质? 。
难度: 中等查看答案及解析
有些金属元素只能通过焰色反应才能鉴定如K、Na,做焰色反应实验所用的铂丝每次用完后都必须洗净,下列溶液可以用来洗铂丝的是
A.稀H2SO4 B.稀HNO3 C.浓H2SO4 D.稀HCl(aq)
难度: 简单查看答案及解析
下列分散系与纳米级微粒在直径上具有相同数量级的是
A.溶液 B.胶体 C. 悬浊液 D.乳浊液
难度: 简单查看答案及解析
合金比纯金属的性能更优良,应用范围更广,下列材料不是合金的是
A.黄铜 B.合金钢 C.硬铝 D. 金箔
难度: 简单查看答案及解析
下列物质的名称和化学式不相符的是
A.铝土矿(Al2O3) B.磁性氧化铁(FeO)
C.铁红(Fe2O3) D.明矾[KAl(SO4)2·12H2O]
难度: 中等查看答案及解析
下列物质按电解质、非电解质、混合物排序正确的是
A.五水硫酸铜、SO2、空气 B.NH3、Cu、空气
C.盐酸、硫酸、胶体 D.氨水、食盐、酒精
难度: 中等查看答案及解析
下列物质不能由化合反应制得的是
A.AlCl3 B .Fe(OH)3 C.NaOH D.Al(OH)3
难度: 中等查看答案及解析
设NA代表阿佛加德罗常数,下列说法正确的是
A.22.4LCO和CO2的混合气体中所含的碳原子数一定是NA
B.Na2O2与CO2反应每生成1mol O2时所转移的电子数为4NA
C.常温常压下,32g O2和32g O3所含氧原子数都是2NA
D.1 mol/L的盐酸溶液中含的离子数为2NA
难度: 中等查看答案及解析
下列离子方程式书写正确的是
A.钠和冷水反应 Na+2H2O=Na++2OH+H2↑
B.Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O
C.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
D.FeCl2溶液通入足量的Cl2反应:Fe2++Cl2=Fe3++2Cl-
难度: 中等查看答案及解析
在强酸性溶液中能大量共存的透明离子组是
A.K+ Na+ NO3- CO32- B.Na十 Fe3+ SCN- SO42-
C.K+ Na十 Cl- AlO2— D.Al3+ Na+ Cl- SO42-
难度: 中等查看答案及解析
下列实验现象描述不正确的是
| 编码 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先融化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔融化,失去光泽,融化的铝并不滴落,好像一层膜兜着 |
| C | 在空气中久置的铝条放入NaOH溶液中 | 铝条立刻产生大量无色气泡,铝条逐渐变细,铝条逐渐发热 |
| D | 在FeCl2溶液中滴入NaOH溶液 | 生成白色沉淀,沉淀很快变为灰绿色,最后变为红褐色 |
难度: 中等查看答案及解析
对于反应8NH3+3Cl2=N2+6NH4Cl,下列说法正确的是
A.N2是还原产物,且还原剂与氧化剂物质的量之比是2∶3
B.N2是氧化产物,且还原剂与氧化剂物质的量之比是2∶3
C.每转移6mol电子就生成22.4L N2
D.NH4Cl是氧化产物,且还原剂与氧化剂物质的量之比是2∶3
难度: 中等查看答案及解析
下列各组物质只用胶头滴管和试管不能鉴别的是
A.KOH溶液与AlCl3溶液 B.NaAlO2溶液与盐酸
C.NaHCO3溶液与盐酸 D.Na2CO3溶液与盐酸
难度: 中等查看答案及解析
将质量为8g的铁棒插入到一定浓度的AgNO3 溶液中,充分反应后取出铁棒,经洗涤、干燥、称量得知铁棒的质量增加到16g,参加反应的AgNO3的物质的量为
A. 0.09mol B.0.1 mol C. 0.2 mol D.无法计算
难度: 中等查看答案及解析
一块质量为0.92g金属钠投入到100ml物质的量浓度0.1mol/L的AlCl3溶液中,反应得到的生成物是
A.H2、Al(OH)3 B.H2、NaAlO2
C.H2、NaAlO2、NaCl D.H2、Al(OH)3、NaCl
难度: 中等查看答案及解析
把NaHCO3和Na2CO3·10H2O混和物6.56g溶于水制成100mL溶液,其中c(Na+)=0.5mol/L。在该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为
A.2.93 g B.5.85 g C.6.56g D.无法确定
难度: 中等查看答案及解析
现有A、B两个烧杯中分别盛有100ml3mol/L的盐酸和100ml3mol/L的氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成H2的体积比是3:5,则加入铝粉的质量为
A.1.8g B.3.6g C.5.4g D.4.5g
难度: 中等查看答案及解析
两种金属的混合物共15g,跟足量的盐酸反应时,恰好得到11.2L氢气(标况)。下列各组金属不可能构成上述条件的混合物的是
A.镁和银 B.铁和锌 C.铝和铁 D.镁和铁
难度: 中等查看答案及解析
120mL浓度为1 mol//L的Na2SO3溶液,恰好与100mL浓度为0. 4 mol//L的K2Cr2O7溶液完全反应,在还原产物中Cr元素的化合价
A.+3 B.+1 C.+4 D.+2
难度: 中等查看答案及解析
(1)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个化学反应方程式表示其变化:① ,② 。
(2)金属钠着火时要用 灭火,请写出Na2O2与水的离子方程式
(3)用离子方程式表示实验室用Al2(SO4)3溶液制Al(OH)3的最佳方案 ,制备时为什么不能用NaOH溶液 (用化学方程式解释)。
难度: 中等查看答案及解析
如图,已知有以下物质相互转化

(1) A转化为B及气体这步反应中应加入的试剂是(填化学式) ,C溶液中溶质的化学式 。
(2)写出由E转变成F的化学方程式 。
(3)写出检验G溶液中阳离子的离子方程式 ;向G溶液中加入A的有关离子反应方程式是 。
(4) 有一瓶存放时间较长的B溶液,某学生怀疑其有部分因氧化而变质,如果有变质,应如何除去变质的杂质? 。
难度: 中等查看答案及解析
Ⅰ.常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应。小明设计如下实验探究铁粉与水蒸气反应后的气体产物。
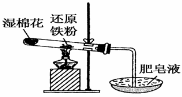
(1)试管尾部放一团湿棉花的目的是_____ 。
(2)铁与水蒸气反应的化学方程式
(3)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。
Ⅱ.某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:
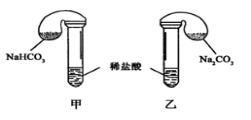
(1)各组反应开始时,_____________装置中的气球体积先变大,该装置中反应的离子方程式是_________________________。
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格。
| 试剂用量 | 实验现象(气球体积变化)) | 分析原因 | |
| 第 ① 组 | 42 g NaHCO3 53 g Na2CO3 300mL4 mol/L盐酸 | 甲中气球与乙中 气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)=n (Na2CO3) V甲(CO2)=V乙(CO2) |
| 第 ② 组 | 42 g NaHCO3 53 g Na2CO3 300mL3 mol/L盐酸 |
难度: 困难查看答案及解析
将3.9gMg、Al合金溶于一定物质的量浓度的HCl溶液400mL中,刚好完全反应,经检测合金和盐酸都无剩余,再向反应后的溶液中加入1mol/L的NaOH溶液后,生成沉淀,当加入400mL NaOH溶液时沉淀量恰好达到最大。请求
(1)所用盐酸的物质的量浓度为多少mol/L
(2)生成的沉淀的质量最大值是多少g?
(3)原合金中Mg的质量百分含量(计算结果保留一位小数点)。
难度: 中等查看答案及解析