-
决定元素种类的是原子的( )
A.质子数
B.中子数
C.电子数
D.最外层电子数难度: 中等查看答案及解析
-
下列金属中,活动性最强的是( )
A.镁
B.铜
C.锌
D.铝难度: 中等查看答案及解析
-
汽车尾气中的CO在四氧化三钴(CO3O4)纳米棒的催化作用下,低温即与O2反应生成CO2.下列关于该反应的说法中,不正确的是( )
A.反应类型为化合反应
B.可降低汽车尾气对大气的污染
C.反应前后Co3O4质量改变
D.反应前后碳元素的化合价改变难度: 中等查看答案及解析
-
每年5月31日为世界无烟日.吸烟有害健康,烟气中的一种有毒气体是( )
A.O2
B.N2
C.CO
D.CO2难度: 中等查看答案及解析
-
氢氧化钠是重要的化工原料,其俗称是( )
A.纯碱
B.烧碱
C.小苏打
D.熟石灰难度: 中等查看答案及解析
-
下列物质中,能用作钾肥的是( )
A.K2SO4
B.CO(NH2)2
C.NH4NO3
D.Ca(H2PO4)2难度: 中等查看答案及解析
-
下列物质性质的表述中,属于化学性质的是( )
A.氧气无色无味
B.铝呈银白色
C.蔗糖易溶于水
D.碳酸易分解难度: 中等查看答案及解析
-
能与无色硝酸银溶液反应,使溶液变为蓝色的金属是( )
A.铝
B.铁
C.铜
D.银难度: 中等查看答案及解析
-
下列依据实验目的所设计的实验操作中,正确的是( )
选项 实验目的 实验操作 A 检验NaCl中含有Na2CO3 加水溶解 B 鉴别NaOH和Ca(OH)2溶液 加Na2CO3溶液 C 除去CaO中的CaCO3 加足量稀盐酸 D 除去CO2中的CO 通入足量NaOH溶液
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
空气中体积分数约占78%的气体是( )
A.氧气
B.氮气
C.二氧化碳
D.稀有气体难度: 中等查看答案及解析
-
下列物质中,含有氧分子的是( )
A.O2
B.H2O
C.CO2
D.SO2难度: 中等查看答案及解析
-
下列物质敞口放置,质量会减轻的是( )
A.氢氧化钠
B.浓硫酸
C.浓盐酸
D.碳酸钙难度: 中等查看答案及解析
-
下列变化中,属于化学变化的是( )
A.矿石粉碎
B.纸张燃烧
C.酒精挥发
D.冰雪融化难度: 中等查看答案及解析
-
已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则核外电子数为( )
A.2
B.6
C.8
D.14难度: 中等查看答案及解析
-
垃圾分类从你我他开始.废弃塑料瓶属于( )
A.
可回收物
B.
有害垃圾
C.
厨余垃圾
D.
其他垃圾难度: 中等查看答案及解析
-
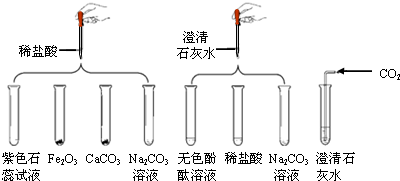
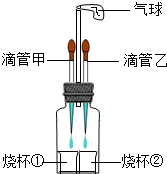
根据下图所示实验分析得出的结论中,不正确的是( )
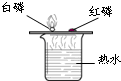
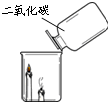
A.甲烷燃烧生成二氧化碳和水 B.铁能在氧气中燃烧 C.白磷的着火点比红磷的低 D.二氧化碳的密度比空气大,
不燃烧也不支持燃烧
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列操作中,可以将空气、氧气和二氧化碳三瓶气体鉴别开的是( )
A.观察气体的颜色
B.伸入燃着的木条
C.闻气体的气味
D.倒入澄清的石灰水难度: 中等查看答案及解析
-
工业上用甲和乙反应制备燃料丙.根据下列微观示意图得出的结论中,正确的是( )

A.甲的化学式为CH2
B.反应中甲、乙、丙的分子个数比为2:1:1
C.甲、乙、丙都是有机物
D.丙中C、H、O元素的质量比为12:3:8难度: 中等查看答案及解析
-
氨基钠(NaNH2)是合成维生素A的原料.工业上将钠于97~100℃熔融,向反应容器中缓慢通入无水的液氨(NH3),再加热至
350~360℃生成氨基钠和氢气.下列说法中,不正确的是( )
A.钠可能与水反应
B.钠的熔点比铁的熔点低
C.维生素A中一定含有钠元素
D.反应的化学方程式为:2Na+2NH32NaNH2+H2
难度: 中等查看答案及解析
-
下列4个图象能正确反映对应变化关系是( )
A.
向一定量稀H2SO4中加入NaOH溶液
B.
用酒精灯加热一定量KMnO4固体
C.
向一定量澄清石灰水中加入
Na2CO3溶液
D.
向盛有MnO2的烧杯中
加入H2O2溶液难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.
矿泉水
B.
苏打水
C.
白醋
D.
蒸馏水难度: 中等查看答案及解析
-
下列做法中,不利于保护水资源的是( )
A.使用节水型马桶
B.合理使用农药和化肥
C.生活污水任意排放
D.工业废水处理达标后排放难度: 中等查看答案及解析
-
小刚测定了下列4种日用品的pH,其中呈酸性的是( )
日用品 A.洁厕灵 B.洗涤灵 C.洗发水 D.消毒液 pH 1 7 9 12
A.洁厕灵
B.洗涤灵
C.洗发水
D.消毒液难度: 中等查看答案及解析
-
下列实验操作中,正确的是( )
A.
倾倒液体
B.
点燃酒精灯
C.
取用固体粉末
D.
过滤难度: 中等查看答案及解析
-
下列化学方程式中,书写正确的是( )
A.2H2O=2H2↑+O2↑
B.H2SO4+NaOH=NaSO4+H2O
C.Fe+HCl=FeCl2+H2↑
D.2KMnO4K2MnO4+MnO2+O2↑
难度: 中等查看答案及解析
 纯棉帽子 B.
纯棉帽子 B. 羊毛衫 C.
羊毛衫 C. 涤纶运动裤
涤纶运动裤