-
下列变化中,属于化学变化的是( )
A.电灯通电后,灯丝发光发热
B.在潮湿的空气中,铁钉生锈
C.含碳和氢的石蜡受热时熔化
D.在研钵内,蓝色的块状胆矾被研碎难度: 中等查看答案及解析
-
下列各组物质中,前者属于金属单质后者属于氧化物的组合是( )
A.铜绿和液态氧
B.氦和一氧化碳
C.碘和氯化钾
D.汞和冰难度: 中等查看答案及解析
-
为了探究水电解的微观过程,某同学做了一些下图所示的分子、原子的模型,若用“
”表示氢原子,用“
”表示氧原子,其中能保持氢气的化学性质的粒子是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
对下列现象的解释中,正确运用了原子--分子论的是( )
现象 解释 A 在远处即能闻到白酒的香气 白酒的分子是可分的 B 碘蒸气的凝华 碘分子的体积很小 C 氧化汞在加热时被分解成两种物质 构成氧化汞分子的汞原子和氧原子重新组合,每2个氧原子结合成1个氧分子,许多个氧分子构成氧气,许多个汞原子直接构成汞 D 一般物体会热胀冷缩 构成物质的分子质量非常小
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
不同种元素最本质的区别是( )
A.质子数不同
B.中子数不同
C.相对原子质量不同
D.电子数不同难度: 中等查看答案及解析
-
下列化学反应中,既不属于化合反应,也不属于分解反应,还不属于置换反应的是( )
A.Cu2(OH)2CO32CuO+H2O+CO2↑
B.3Fe+4H2O(气)Fe3O4+4H2
C.2C22H46+67O244CO2+46H2O
D.2C+O22CO
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.由两种或两种以上的元素组成的纯净物是化合物
B.元素可以以单质状态存在,也可以以化合物状态存在
C.红磷、白磷都是仅由磷元素组成的单质,但它们的性质有所不同
D.纯净物一定由同种分子构成难度: 中等查看答案及解析
-
下列说法中,不正确的是( )
A.在氯酸钾的分解反应中,二氧化锰起催化作用
B.要使氯酸钾受热分解出氧气,必须加入二氧化锰,否则就不能发生反应
C.细铁丝在氧气里燃烧时,火星四射,生成黑色固体
D.可以用向上排空气集气法收集氧气难度: 中等查看答案及解析
-
所含氮元素的质量相等时,下列四种化肥中质量最大的是( )
A.(NH4)2SO4
B.NH4Cl
C.CO(NH2)2
D.NH4HCO3难度: 中等查看答案及解析
-
下列各实验操作中,错误的是( )
A.
液体的倾倒
B.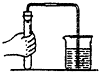
检查装置的气密性
C.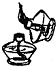
点燃酒精灯
D.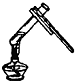
加热试管里的液体难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A.凡是在通常条件下不能燃烧的物质,都是不能与氧气反应的物质
B.氧气很活泼,在常温时能与所有物质发生剧烈的化学反应
C.可燃物在纯净的氧气中燃烧比在空气中燃烧要剧烈
D.发生缓慢氧化的物质一定会自燃难度: 中等查看答案及解析
-
人在剧烈运动后,血液中会产生较多的乳酸(化学式为C3H6O3),使肌肉酸痛.放松-段时间后,由于乳酸与吸入的氧气反应生成二氧化碳和水,从而使肌肉的酸痛感消失.下列关于乳酸及其与氧气发生的反应表述正确的是( )
A.乳酸是由碳元素、氢元素、氧元素组成的
B.乳酸由3个碳原子、6个氢原子和3个氧原子构成
C.乳酸中碳元素的质量分数为40%
D.乳酸与氧气反应的化学方程式为2C3H6O3+5O2=6CO2+6H2O难度: 中等查看答案及解析
-
下列说法中,不正确的是( )
A.空气中体积分数最大的气体为氮气
B.地壳中质量分数最大的元素为氧元素
C.相同条件下,氢气是密度最小的气体
D.不能支持红磷燃烧的气体一定是氮气难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A.水通电可以被分解及氢气、氧气在一定条件下能化合,这些事实都能证明化学反应中分子可以再分
B.化学反应前后,物质的质量总和一定相等
C.化学反应前后,物质的分子个数总和一定相等
D.某化合物在纯氧中燃烧生成CO2和SO2,该化合物中一定含有碳、硫、氧三种元素难度: 中等查看答案及解析
-
下列说法中,不正确的是( )
A.在点燃条件下,质量比为1:1的硫和氧气恰好完全化合成二氧化硫
B.在点燃条件下,质量比为1:2的碳和氧气恰好完全化合成二氧化碳
C.在点燃条件下,分子个数比为2:1的氢气和氧气恰好完全化合成水
D.20g(NH4)2SO4中所含氮、氢元素的质量之比与20gNH4Cl中所含氮、氢元素的质量之比是相同的难度: 中等查看答案及解析