-
纯水在20℃和80℃时的pH
A.前者大 B.后者大 C.相等 D.无法确定
-
下列化合物属于弱电解质的是
A.HClO4 B.Ba(OH)2 C.CO2 D.HF
-
下列关于强、弱电解质的叙述,错误的是
A.强电解质在溶液中完全电离,不存在电离平衡
B.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
C.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同
D.纯净的强电解质在液态时,有的导电,有的不导电
-
氨水中所含有的分子和离子有①NH4+ ②H2O ③NH3 ④NH3·H2O ⑤H+ ⑥OH-
A.①②③ B.②③④⑤ C.②③④⑤⑥ D.①②③④⑤⑥
-
25 ℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
-
下列能大量共存的离子组是
A.NH4+、Mg2+、OH-、Cl- B.Ba2+、K+、SO42-、NO3-
C.Al3+、Cu2+、SO42-、Cl- D.Na+、Al3+、Cl-、AlO2-
-
下列过程或现象与盐类水解无关的是
A.纯碱溶液去油污 B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深 D.泡沫灭火器灭火
-
在蒸发皿中加热蒸干再灼烧下列物质的溶液,可以得到该物质固体的是
A.氯化铝 B.碳酸氢钠 C.氯化亚铁 D.硫酸铜
-
下列导电能力最差的电解质
A.熔融的NaOH B.硫磺 C.石墨棒 D.KNO3晶体
-
下列各式中属于正确的水解反应离子方程式的是
A.CH3COOH + OH-  CH3COO- +H2O
CH3COO- +H2O
B.S2-+2H2O H2S+2OH-
H2S+2OH-
C.CH3COOH+H2O CH3COO- +H3O+
CH3COO- +H3O+
D.NH4++H2O NH3· H2O+H+
NH3· H2O+H+
-
下列关于电离平衡常数(K)的说法中正确的是
A.在一定温度,相同浓度时电离平衡常数(K)越大可以表示弱电解质电离程度越大
B.电离平衡常数(K)与温度无关
C.不同浓度的同一弱电解质,其电离平衡常数(K)不同
D.多元弱酸各步电离平衡常数相互关系为K1<K2<K3
-
把下列溶液,溶液的pH值不会改变的是
A.CH3COOH溶液 B.NaCl溶液 C.NaOH溶液 D.FeCl3溶液
-
常温下某溶液中由水电离产生的[H+]=1×10-5mol·L-1,则下列叙述正确的是
A.一定是碱溶液
B.一定是酸溶液
C.由水电离出的[OH-]=1×10-9mol·L-1
D.pH值可能为9也可能为5
-
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是
CH3COO-+H+,对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向正反应方向移动
B.加水,反应速率增大,平衡向逆反应方向移动
C.滴加少量0.1mol/L HCl溶液,溶液中c(H+)减少
D.加入少量CH3COONa固体,平衡向正反应方向移动
-
室温时,下列混合溶液的pH一定小于7的是
A.pH=3的盐酸和pH=11的氨水等体积混合
B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合
C.pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合
D.pH=3的硫酸和pH=11的氨水等体积混合
-
25℃时,向V mL pH=a的盐酸中,滴加10V mL pH=b的NaOH溶液,所得溶液中Cl-的物质的量恰好等于Na+的物质的量,则a+b的值是
A.15 B.14 C.13 D.不能确定
-
下列关于醋酸钠溶液的说法中正确的是
A.溶液呈酸性
B.c(H+)= c(CH3COO-)+ c(OH-)
C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
-
在相同温度下,等体积等物质的量浓度的4种稀溶液:①Na2SO4、②H2SO4、③NaHSO4、④Na2S中所含离子种类由多到少的顺序是
A.①=④>③=② B.④=①>③>②
C.①>④>③>② D.④>①=③>②
-
25 ℃时,将0.23 g钠投入到100 g水中充分反应,假设反应后溶液体积为100 mL,则该溶液的pH为
A.1 B.13 C.12 D.10
-
向稀硫酸溶液中逐渐加入氨水,当溶液中c(NH4+)=2c(SO42-)时,溶液的pH
A.等于7 B.大于7 C.小于7 D.无法判断
-
常温下pH=2的两种酸溶液A和B,分别加水稀释1000倍,其pH值与所加水的体积变化如图所示。下列结论正确的是

A.酸B比酸A的电离度大
B.A为弱酸,B为强酸
C.酸B的物质的量浓度比A的小
D.A酸比B酸易电离
-
下列各溶液中,微粒的物质的量浓度关系正确的是
A.1.0 mol/L Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+)+ 2c(H2CO3)
B.1.0 mol/L NH4Cl溶液:c(NH4+) = c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+) >c(CH3COO-)>c(H+)>c(OH-)
D.1 mol/L CH3COONa溶液,c(CH3COO-)= 1 mol/L
-
下列说法正确的是
A.在Na2CO3、NaHCO3两溶液中,离子种类不相同
B.在等体积、等物质的量浓度的Na2CO3、NaHCO3两溶液中,阳离子总数相等
C.在NaHCO3和Na2CO3混合溶液中一定有:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
D.在NaHCO3和Na2CO3混合溶液中一定有:2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
-
25℃时,0.1mol/L稀醋酸加水稀释,如图中的纵坐标y可以是
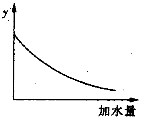
A.溶液的pH B.醋酸的电离平衡常数
C.溶液的导电能力 D.醋酸的电离程度
-
从植物花汁中提取的一种有机物HIn,可做酸碱指示剂,在水溶液中存在电离平衡:HIn(红色) H+ + In-(黄色)△H>0对上述平衡解释不正确的是
H+ + In-(黄色)△H>0对上述平衡解释不正确的是
A.升高温度平衡向正方向移动
B.加入盐酸后平衡向逆方向移动,溶液显红色
C.加入NaOH溶液后平衡向正方向移动,溶液显黄色
D.加入NaHSO4溶液平衡向正方向移动,溶液显黄色

