-
2013年5月,全国科协年会在贵阳举行,其“生态文明与绿色发展”等相关内容为贵阳市生态文明城市建设注入了新的内涵.在生态文明城市建设中,下列做法不当的是( )
A.扩大湿地公园面积,改善空气质量 B.发展城市轨道交通,倡导低碳出行
C.大力发展火力发电,满足用电需求 D.学好化学科学知识,提升科学素养
难度: 简单查看答案及解析
-
对“桂花十里飘香”的下列解释正确的是( )
A.分子在不断运动 B.分子间有间隔 C.分子体积很小 D.分子质量很小
难度: 中等查看答案及解析
-
贵州盛产金银花,从金银花中提取的绿原酸(化学式为C16H18O9)有很高的药用价值.下列有关绿原酸的说法正确的是( )
A.绿原酸属于混合物
B.绿原酸由碳、氢、氧三种元素组成
C.绿原酸的相对分子质量为354g
D.绿原酸中氢元素的质量分数最大
难度: 中等查看答案及解析
-
下列物质的用途与化学反应原理及反应类型对应不相符的是( )
选项 用途 化学反应原理(用方程式表示) 基本反应类型
A H2作燃料 2H2+O2
2H2O 化合反应
B 石灰石制生石灰 CaCO3
CaO+CO2↑ 分解反应
C CO用于炼铁 3CO+Fe2O3
2Fe+3CO2 置换反应
D Al(OH)3用于治疗胃酸过多 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应
难度: 中等查看答案及解析
-
钠和氯气反应生成氯化钠的化学方程式为2Na+Cl2=2NaCl,反应的示意图如图所示.则下列结论不正确的是( )

A.构成物质的粒子有原子、分子和离子
B.化学反应中原子得到或失去的是能量低的电子,并形成相对稳定结构
C.化学反应前后元素种类没有改变
D.元素呈现的化合价与反应中元素原子得失电子及数目有关
难度: 中等查看答案及解析
-
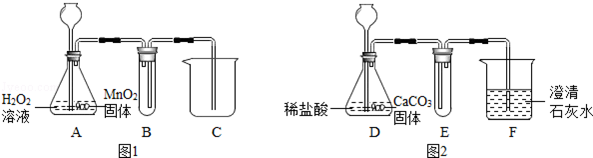
为完成图所示的四个实验中,编号处所指物质的选用正确的是( )

难度: 中等查看答案及解析