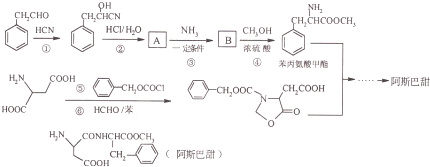
-
现在甲基、羟基、羧基、苯基四种原子团,两两组合形成化合物,其水溶液呈酸性的有( )
A.3种 B.4种 C.5种 D.6种
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述中不正确的是( )
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.常温常压下,22.4L氯气和足量镁粉充分反应,转移的电子数为2NA
难度: 中等查看答案及解析
-
下列离子方程式,正确的是( )
A.硫酸氢铵和氢氧化钠等物质的量混合 NH4++OH-=NH3↑+H2O
B.向Ba(OH)2溶液中加入少量NaHSO3溶液 2HSO3-+Ba2++2OH-=BaSO3↓+SO32- +2H2O
C.将Fe2O3溶于氢碘酸中Fe2O3+6H+=2Fe3++3H2O
D.等物质的量的溴化亚铁跟氯气反应2Fe2++2Br-+2Cl2=2F3++Br2+4Cl-
难度: 中等查看答案及解析
-
下列各组离子能大量共存的是
①“84”消毒液的水溶液中:Fe3+、Cl-、Ca2+、Na+
②加入KSCN显红色的溶液:K+、NH4+、Cl-、S2-
③能够与金属Cu常温下反应放出气体的溶液;Fe3+、Al3+、SO42-、K+
④pH=2的溶液中:NH4+、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HCO3-、MnO4-
A.②③ B.①③ C.①⑤ D.③④
难度: 困难查看答案及解析
-
右图表示4-溴环己烯所发生的4个不同的反应,其中,产物中只含有一种官能团的反应是( )
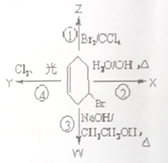
A.①③ B.③④ C.②③ D.①②
难度: 困难查看答案及解析
-
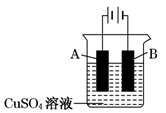
利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
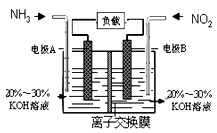
A.电流从右侧电极经过负载后流向左侧电极
B.为使电池持续放电,离子交换膜需选用阴离子交换膜
C.电极A极反应式为:2NH3-6e-=N2+6H+
D.当有4.48L NO2(标准状况)被处理时,转移电子为0.8mol
难度: 困难查看答案及解析
-
将2.7g铝溶解于100mL3mol•L-1NaOH溶液中,然后向所得溶液中加入400mL1mol•L-1的盐酸,最后可得沉淀的质量是( )
A.2.7g B.5.2g C.7.8g D.10g
难度: 中等查看答案及解析