-
“物质的量”实际上是表示( )
A.物质的质量
B.摩尔(mol)
C.粒子的相对质量
D.含有一定数目微观粒子的集体难度: 中等查看答案及解析
-
如果你家里的食用花生油不小心混入大量的水,你将采用下列何种方法分离( )
A.过滤
B.蒸馏
C.分液
D.萃取难度: 中等查看答案及解析
-
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2溶液;④滴入稀盐酸至无气泡产生;⑤过滤;正确的操作顺序是( )
A.③②①⑤④
B.①②③⑤④
C.②③①④⑤
D.③⑤②①④难度: 中等查看答案及解析
-
在无色透明的酸性溶液中,能大量共存的离子组是( )
A.Fe2+、Ag+、S2-、SO42-
B.Mg2+、NH4+、NO3-、Cl-
C.Na+、K+、SO32--、CH3COO-
D.Cu2+、Na+、NO3-、SO42-难度: 中等查看答案及解析
-
能用H++OH-=H2O来表示的化学反应是( )
A.氢氧化镁和稀盐酸反应
B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应
D.二氧化碳通入澄清石灰水中难度: 中等查看答案及解析
-
下列反应既属于离子反应,又属于氧化还原反应的是( )
A.Zn与CuSO4溶液的反应
B.分解氯酸钾制氧气
C.NaOH溶液与盐酸中和
D.MgCl2溶液与KOH溶液产生沉淀难度: 中等查看答案及解析
-
下列离子方程式与化学反应事实一致的是( )
A.石灰石溶于盐酸:CO32-+2H+═H2O+CO2↑
B.硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-═Cu(OH)2↓
C.硫酸氢钠溶液与氢氧化钾溶液反应:H++OH-═H2O
D.硝酸银溶液与氯化钠溶液反应:AgNO3+Cl-═AgCl↓+NO3-难度: 中等查看答案及解析
-
胶体区别于溶液最本质的特征是( )
A.可以通过滤纸
B.有丁达尔效应
C.分散质粒子因吸附而带电荷
D.分散质粒子的直径大小难度: 中等查看答案及解析
-
下列电离方程式书写有误的是( )
A.NaHSO4═Na++H++SO42-
B.NaHCO3═Na++HCO3-
C.CH3COOH═H++CH3COO-
D.Ba(OH)2═Ba2++2OH-难度: 中等查看答案及解析
-
影响一定量气体占有体积大小的主要因素是( )
A.气体分子的微粒数
B.微粒本身的大小
C.微粒的质量
D.微粒间的平均距离难度: 中等查看答案及解析
-
符合图中阴影部分的物质是( )
A.Na2CO3
B.Cu2(OH)2CO3
C.NaCl
D.NaHCO3难度: 中等查看答案及解析
-
下列物质属于非电解质的是( )
A.HCl
B.Fe
C.蔗糖溶液
D.CO2难度: 中等查看答案及解析
-
如图所示,下列实验操作与方法正确的是( )
A.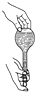 检查容量瓶是否漏水的方法
检查容量瓶是否漏水的方法
B.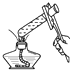 给溶液加热
给溶液加热
C.滴加液体
D.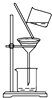 过滤
过滤 难度: 中等查看答案及解析
-
b g某金属与足量的稀硫酸反应,生成该金属的三价正盐和a g氢气.则该金属的相对原子质量为( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
下列物质分类正确的是( )
A.Cu(OH)2难溶于水,属于非电解质
B.SO2能与碱反应生成盐和水,属于酸性氧化物
C.NH4Cl组成中不含金属离子,不属于盐
D.金属铝易导电,属于电解质并且属于强电解质难度: 中等查看答案及解析
-
下列有关氧化还原反应的叙述中正确的是( )
A.有单质参加或有单质生成的反应一定是氧化还原反应
B.氧化还原反应的本质是元素化合价的升降
C.失电子的反应物在反应中作氧化剂,反应中被还原
D.金属单质在化学反应中一定作还原剂难度: 中等查看答案及解析
-
将10g 由Mg、Zn、Fe组成的混合物与40mL稀硫酸恰好完全反应,产生的氢气在标准状况下为5.6L,则三种金属的物质量之和为( )
A.0.5mol
B.0.25mol
C.0.1mol
D.0.125mol难度: 中等查看答案及解析
-
如图是某“泡腾片”的标签.将这样一粒泡腾片放入水中,药片完全溶解,同时产生了大量气泡.这个过程( )
泡腾片
每片含:
碳酸钙 500mg
维生素 1000mg
柠檬酸 1350mg用量… 用法…
A.溶解了500 mg的Ca2+
B.释放了224mL的气体(标准状况)
C.发生了发应:CO32-+2H+=CO2↑+H2O
D.说明了柠檬酸的酸性比碳酸强难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.2.4g镁原子变成离子时,失去的电子数为0.3NA
B.22.4L甲烷(CH4)所含的原子数为5NA
C.常温常压下,28g氮气所含的原子数为2 NA
D.在20℃,1.01×105Pa时,11.2L氧气所含的原子数为NA难度: 中等查看答案及解析
-
为了检验SO42-,甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是( )
A.方案甲:试液白色沉淀
沉淀不溶解
B.方案乙:试液无沉淀(也无气泡)
白色沉淀
C.方案丙:试液无沉淀
白色沉淀
D.方案丁:试液白色沉淀(过滤)
沉淀不溶解
难度: 中等查看答案及解析
-
冬季的降雪为机场和马路带来诸多不便,其中醋酸钾(CH3COOK)是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是( )
A.1 mol CH3COOK的质量为98 g/mol
B.CH3COOK的摩尔质量等于它的相对分子质量
C.一个CH3COOK微粒的质量约为g
D.含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol难度: 中等查看答案及解析
-
阿伏加德罗常数值是NA,标准状况下,若某氧气和氮气的混合气体mg含有b个分子,则ng该混合气体在标准状况下的体积是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
20℃时,食盐的溶解度是36g,根据这句话的含义,判断下列说法中正确的是( )
A.100 g水溶解36 g食盐恰好能配成饱和溶液
B.20℃时,100 g食盐饱和溶液里含有36 g食盐
C.20℃时,把136 g食盐饱和溶液蒸干可得到36 g食盐
D.饱和食盐水中溶质、溶剂和溶液的质量比为36:100:136难度: 中等查看答案及解析
-
下列各组中两种物质在溶液中的反应可用同一离子方程式表示的是( )
A.Cu(OH)2+HCl; Cu(OH)2+CH3COOH
B.NaHCO3+H2SO4; Na2CO3+HCl
C.NaHCO3+NaOH; Ca(HCO3)2+NaOH
D.BaCl2+H2SO4; Ba(OH)2+Na2SO4难度: 中等查看答案及解析
-
已知反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O下列说法不正确的是( )
A.Cl2既是氧化剂 也是还原剂
B.被氧化的氯原子数是被还原的氯原子数的5倍
C.氧化剂和还原剂的质量比是1:5
D.NaCl是还原产物,NaClO3氧化产物难度: 中等查看答案及解析