-
下列关于碳原子的成键特点及成键方式的理解中正确的是( )
A.饱和碳原子不能发生化学反应
B.碳原子只能与碳原子形成不饱和键
C.具有六个碳原子的苯与环己烷的结构不同
D.五个碳原子最多只能形成四个碳碳单键
难度: 中等查看答案及解析
-
下列元素原子半径最接近的一组是( )
A.Ne、Ar、Kr、Xe B.Mg、Cu、Sr、Ba
C.B、C、N、O D.Cr、Mn、Fe、Co
难度: 简单查看答案及解析
-
X与Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Y与Z两元素的核外电子层数相同,Z元素的第一电离能大于Y元素的第一电离能,则X、Y、Z的原子序数
A. X>Y>Z B. Y>X>Z
C. Z>X>Y D. Z>Y>X
难度: 简单查看答案及解析
-
下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2 ③
④CH≡CH ⑤NH3 ⑥CH4
A. ①②③ B. ①⑤⑥ C. ②③④ D. ③⑤⑥
难度: 中等查看答案及解析
-
根据下表中所列的键能数据,判断下列分子中最不稳定的是( )
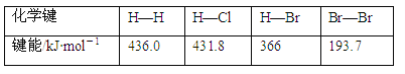
A. HCl B. HBr C. H2 D. Br2
难度: 中等查看答案及解析
-
下列给出的几种氯化物的熔点和沸点:
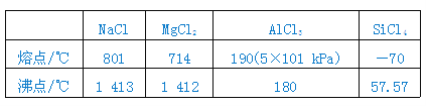
据表中所列数据判断下列叙述与表中相吻合的是( )
A. AlCl3在加热条件下能升华 B. SiCl4晶体属于原子晶体
C. AlCl3晶体是典型的离子晶体 D. NaCl的晶格能比MgCl2小
难度: 中等查看答案及解析
-
有关核外电子运动规律的描述错误的是
A. 核外电子质量很小,在原子核外作高速运动
B. 核外电子的运动规律与普通物体不同,不能用牛顿运动定律来解释
C. 在电子云示意图中,通常用小黑点来表示电子绕核作高速圆周运动
D. 在电子云示意图中,小黑点密表示电子在核外空间单位体积内电子出现的机会多
难度: 简单查看答案及解析
-
4p轨道填充一半的元素,其原子序数是( )
A. 15 B. 33 C. 35 D. 51
难度: 中等查看答案及解析
-
关于CO2与CS2的下列说法正确的是( )
A. 它们互为等电子体 B. CO2为直线形而CS2为V形
C. 它们分子中的化学键类型不同 D. CS2比CO2稳定
难度: 中等查看答案及解析
-
下列各能层中不包含p能级的是( )
A. N B. M C. L D. K
难度: 中等查看答案及解析
-
下列关于晶体的说法正确的组合是 ( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
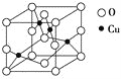
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻

⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A. ①②③⑥ B. ①②④ C. ③⑤⑦ D. ③⑤⑧
难度: 困难查看答案及解析
-
在金刚石的晶体中,含有由共价键形成的碳原子环,其中最小的环上所需碳原子数及每个碳原子上任意两个C--C键间的夹角是( )
A.6个120° B.5个108° C.4个109°28′ D.6个109°28′
难度: 简单查看答案及解析
-
下列有关元素周期表的说法中不正确的是( )
A. 在元素周期表中共有7个周期
B. 元素周期表中有三个短周期
C. 第二周期共有8种元素
D. 第三周期元素全部是金属元素
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 分子晶体中的每个分子内一定含有共价键
B. 原子晶体中的相邻原子间只存在非极性共价键
C. 离子晶体中可能含有共价键
D. 金属晶体的熔点和沸点都很高
难度: 中等查看答案及解析
-
下列说法错误的是( )
A. 离子晶体中阴阳离子间的作用力为静电引力
B. 离子键没有方向性和饱和性
C. 在氯化铯晶体中无CsCl分子单独存在
D. CaF2晶胞中F-的配位数为4
难度: 中等查看答案及解析
-
1999年4月,比利时查出污染鸡的根源是生产鸡饲料的油脂被二恶英所污染,二恶英是两大芳香族化合物的总称。其中四氯代二苯并二恶英毒性最大,其结构简式为:
下列有关该化合物的说法中正确的是( )
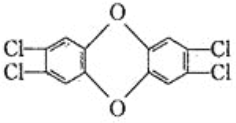
A. 分子式为C12H8O2Cl4
B. 是一种可溶于水的气体
C. 是最危险的致癌物之一
D. 是一种多卤代烃
难度: 中等查看答案及解析
-
下列物质中不能与溴水发生化学反应的是
A. 苯酚 B. 苯乙烯 C. 丙炔 D. 乙烷
难度: 中等查看答案及解析
-
分别将下列物质滴入苯酚溶液中,产生白色沉淀的是
A.浓溴水 B.氢氧化钠溶液
C.稀盐酸 D.氯化铁溶液
难度: 中等查看答案及解析
-
中草药秦皮中含有的七叶树内酯(
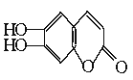 碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )A. 3mol Br22mol NaOH B. 3mol Br24mol NaOH
C. 2mol Br23mol NaOH D. 4mol Br24mol NaOH
难度: 中等查看答案及解析
-
下列属于分离、提纯固态有机物的操作的是 ( )
A. 蒸馏 B. 萃取 C. 重结晶 D. 分液
难度: 简单查看答案及解析
-
化学家们合成了一种新物质——五星烷,其键线式如图所示。下列有关五星烷的说法正确的是( )
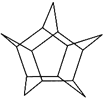
A. 五星烷与乙烷互为同系物 B. 五星烷的化学式为C15H20
C. 五星烷的分子中含有7个五元环 D. 五星烷的一氯代物有3种
难度: 中等查看答案及解析
-
如图照片显示:一只可爱小猫站在一块高分子合成材料上,下面烈火灼烧而小猫却若无其事,这说明此高分子材料一定具有的性质是( )

A. 良好的绝缘性
B. 良好的绝热性
C. 良好的导热性
D. 熔点低
难度: 简单查看答案及解析
-
以下不属于酯类物质的是
A.甘氨酸 B.硝化甘油 C.脂肪 D.硝酸纤维
难度: 简单查看答案及解析
-
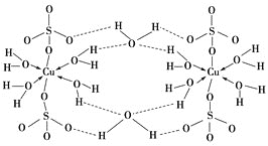
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是 ( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
难度: 中等查看答案及解析
-
下列反应中,液体植物油不能发生的有( )
A. 加成反应 B. 氧化反应
C. 水解反应 D. 消去反应
难度: 中等查看答案及解析
-
苏丹红是很多国家禁止用于食品生产的合成色素。结构简式如右图。关于苏丹红说法错误的是( )
A. 分子中含一个苯环和一个萘环 B. 属于芳香烃
C. 能被酸性高锰酸钾溶液氧化 D. 能溶于苯
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. 含有羟基的有机物称为醇
B. 能发生银镜反应的有机物都是醛
C. 苯酚俗称石炭酸,酸性比碳酸强
D. 酯类在碱性条件下的水解程度大于酸性条件下的水解程度
难度: 中等查看答案及解析
-
乙酸是生活中常见的一种有机物,下列关于乙酸的说法中正确的是
A. 乙酸的官能团为-OH B. 乙酸的酸性比碳酸弱
C. 乙酸能够与金属钠反应产生氢气 D. 乙酸能使紫色的石蕊溶液变蓝
难度: 简单查看答案及解析
-
酯化反应是有机化学中的一类重要反应,下列对于酯化反应理解不正确的是( )
A. 酯化反应是酸和醇生成酯和水的反应 B. 酯化反应是中和反应
C. 酯化反应是有限度的 D. 酯化反应是一般需要催化剂
难度: 中等查看答案及解析