-
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
A.两种气体的压强相等
B.O2比O3质量小
C.两种气体的分子数目相等
D.两种气体的氧原子数目相等难度: 中等查看答案及解析
-
下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A.进行蒸发操作时,蒸发皿中出现大量固体时,即可停止加热
B.进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大难度: 中等查看答案及解析
-
下列物质分类正确的是( )
A B C D 酸 HCl气体 硫酸 醋酸 盐酸 碱 熟石灰 烧碱 纯碱 NH3•H2O 盐 小苏打 胆矾 碱式碳酸铜 NaHSO4 氧化物 水 过氧化氢 Al2O3 KClO3 电解质 Cl2 液态HCl NaCl溶液 H2O
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
为了除去已滤去泥沙的粗盐水中的 Ca2+、Mg2+、SO42-,可将该粗盐水进行下列五项操作.其中正确的操作顺序是( )
①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量 Na2CO3溶液 ⑤加过量 BaCl2溶液.
A.①④②⑤③
B.④①②⑤③
C.②⑤④①③
D.⑤②④③①难度: 中等查看答案及解析
-
在碱性溶液中能大量共存,并且溶液为无色透明的是( )
A.Na+、K+、MnO4-、SO42-
B.NH4+、Na+、NO3-、Cl-
C.K+、Ba2+、NO3-、Cl-
D.Mg2+、Fe3+、Cl-、NO3-难度: 中等查看答案及解析
-
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记的是( )
A.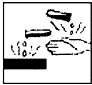
B.
C.
D.难度: 中等查看答案及解析
-
化学试验中必须注意安全,以下实验操作或事故处理中正确的是( )
①在点燃H2、CO、CH4等易燃气体前,必须检验气体的纯度
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中并不断用玻璃棒搅拌
③浓碱液对皮肤有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体应不超过试管容积的
⑤点燃装满酒精的酒精灯.
A..①②③④
B.仅①②③
C.仅①②
D.仅①③难度: 中等查看答案及解析
-
如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )
A.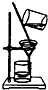
B.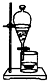
C.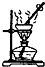
D.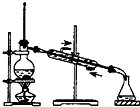
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.金属钠加入硫酸铜溶液中可置换出铜
B.单质钠在空气中加热生成白固体氧化钠
C.因煤油的密度比钠小,钠不与煤油反应,所以钠可保存在煤油中
D.金属钠露置在空气中最终转化为NaOH固体难度: 中等查看答案及解析
-
只给出下表甲和乙中对应的量,不能求出相应物质的物质的量的是:( )
① ② ③ ④ ⑤ 甲 物质粒
子数标准状况下气体摩尔体积 固体体积 溶液中溶质质量分数 非标准状况下物质的质量 乙 阿伏加德罗常数 标准状况下气体体积 固体密度 溶液的体积 物质的
摩尔质量
A.②③
B.①④
C.③④
D.③⑤难度: 中等查看答案及解析
-
根据下列反应,判断氧化性强弱正确的是( )
①2H2S+O2=2S+2H2O ②Na2S+I2=2NaI+S ③4NaI+O2+2H2O=2NaOH+2I2.
A.O2>I2>S
B.O2>S>I2
C.I2>O2>S
D.S>I2>O2难度: 中等查看答案及解析
-
单质X和Y相互反应生成
,现有下列叙述:①X被氧化;②X是氧化剂;③X具有氧化性;④Y2-是还原产物;⑤Y2-具有还原性;⑥X2+具有氧化性;⑦Y的氧化性比X2+的氧化性强.其中正确的是( )
A.①②③④
B.①④⑤⑥⑦
C.②③④
D.①③④⑤难度: 中等查看答案及解析
-
NA为阿伏伽德罗常数,下列叙述错误的是( )
A.18gH2O中含的质子数为10NA
B.标准状况下,22.4L空气含有NA个单质分子
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA难度: 中等查看答案及解析
-
能正确表示下列反应的离子方程式是( )
A.利用腐蚀法制作印刷线路板:Fe3++Cu=Fe2++Cu2+
B.石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓
C.碳酸钙溶于醋酸:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32-难度: 中等查看答案及解析
-
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O═H2SO4+2HBr相比较,水的作用相同的是( )
A.2Na+2H2O═2NaOH+H2↑
B.4Fe(OH)2+O2+2H2O═4Fe(OH)3
C.2F2+2H2O═4HF+O2
D.2H2O2H2+O2↑
难度: 中等查看答案及解析
-
V L硫酸铝溶液中含Al3+的质量为m g,则溶液中SO42-的物质的量浓度为( )
A.mol•L-1
B.mol•L-1
C.mol•L-1
D.mol•L-1
难度: 中等查看答案及解析
-
100mL0.03mol/LNa2SO4溶液和50mL0.02mol/LAl2(SO4)3溶液混合(不考虑水的电离),下列说法中正确的是(不考虑混合后溶液体积的变化)( )
A.混合液中c(SO42-)为0.04mol∙L-1
B.原Al2(SO4)3溶液中c(Al3+)与100mL0.02mol∙L-1Al(NO3)3中c(Al3+)相等
C.混合后的溶液中含有0.003molNa+
D.混合后溶液中c(Na+)为0.02mol/L难度: 中等查看答案及解析
-
将钠、镁、铝各0.2mol 分别放入100mL 1mol/L的盐酸中,同温同压下产生的气体体积比是( )
A.1:2:3
B.6:3:2
C.2:1:1
D.1:1:1难度: 中等查看答案及解析
-
质量分数为w1、物质的量浓度为c1的硫酸溶液与质量分数为w2、物质的量浓度为c2的硫酸溶液相比,如w1=2w2,则c1与c2的关系正确的是( )
A.c1=2c2
B.c1>2c2
C.c1<2c2
D.c2<c1<2c2难度: 中等查看答案及解析

