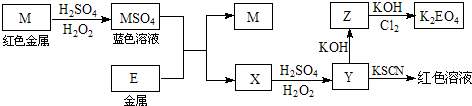
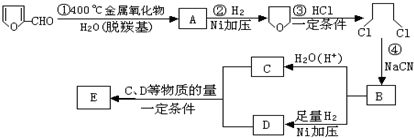
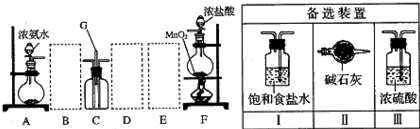
-
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
A.常温下,1 L 0.1 mol•L-1的NH4NO3溶液中氮原子数为0.2 NA
B.盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol
C.在18g18O2中含有NA个氧原子
D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1 mol•L-1难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物
B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力
C.氧气和臭氧间的相互转化属于氧化还原反应
D.常温下,可以用铝制容器贮藏浓硫酸和浓硝酸,其原理相同难度: 中等查看答案及解析
-
下列实验中操作及现象与结论对应关系正确的一组是( )
实验操作 实验现象 实验结论 A 适量二氧化碳通入氯化钡溶液中 产生白色沉淀 碳酸的酸性比盐酸弱 B 二氧化硫通入溴水中 溶液褪色 二氧化硫有漂白性 C 取少量某无色溶液,先滴加氯水,再加入少量四氯化碳,振荡、静置 溶液分层,下层呈紫红色 原无色溶液中一定有碘离子 D 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 产生红色沉淀 淀粉水解可生成葡萄糖
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
下列溶液中各微粒的浓度关系正确的是( )
A.0.1 mol•L-1Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S)
B.0.l mol•L-1pH=9的NaNO2溶液中:c(Na+)>c(NO2-)>c(OH-)>c(H+)
C.等pH的氨水、NaOH溶液、Ba(OH)2溶液中:c(NH4+)=c(Na+)=c(Ba2+)
D.向NH4HCO3溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)=c(HCO3-)+c(CO32-)难度: 中等查看答案及解析
-
恒温恒压下1molA和nmolB在一个容积可变的容器中发生如下反应:A(g)+2B(g)⇌2C(g),一段时间后达到平衡,生成amolC.则下列说法中正确的是( )
A.物质A、B的转化率之比一定是1:2
B.若起始时放入3molA+3nmolB,则达平衡时生成3amolC
C.起始时刻和达平衡后容器中的压强比为
D.当v正(A)=2v逆(C)时,可断定反应达平衡难度: 中等查看答案及解析
-
有一种烃的分子结构如图所示,有关该分子的说法不正确的是( )
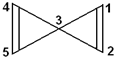
A.该烯烃的分子式为C5H4
B.该分子中1、2、4、5四个碳原子可能在同一平面上
C.该烃的二氯代物同分异构体有2种
D.与其互为同分异构体,且只含三键的链烃只有2种难度: 中等查看答案及解析
-
英国研究人员2007年8月30日发表报告认为,全球将有1.4亿人因为用水而受到砷中毒之害,导致更多的人患癌症.海带含砷超标,经水浸泡24小时后,其含砷量才能达到食用安全标准,下列对砷(As)的有关判断正确的是( )
A.砷原子序数为33,它与铝为同主族
B.砷的原子半径小于磷的原子半径
C.砷化氢的稳定性比溴化氢的强
D.砷酸的酸性比硫酸的弱难度: 中等查看答案及解析
-
一定质量的Al、Mg合金与适量的稀硫酸恰好完全反应,将反应后的溶液整个蒸干,所得固体(不含结晶水)质量比原固体增加了7.2g,则该合金的物质的量可能为( )
A.0.05mol
B.0.06mol
C.0.08mol
D.0.09mol难度: 中等查看答案及解析