-
空气成分中,体积分数约占78%的是
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
难度: 简单查看答案及解析
-
下列符合质量周恒定律的是
A.矿石粉碎 B.纸张燃烧 C.酒精挥发 D.冰雪融化
难度: 简单查看答案及解析
-
决定元素种类的是
A.中子数 B.质子数 C.核外电子数 D.最外层电子数
难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是
A.石灰水 B.空气 C.生铁 D.干冰
难度: 中等查看答案及解析
-
下列金属中,活动性最强的是
A.镁 B.铜 C.锌 D.铝
难度: 简单查看答案及解析
-
每年5月31日为世界无烟日。吸烟有害健康,烟气中的一种有毒气体是
A.O2 B.N2 C.CO D.CO2
难度: 简单查看答案及解析
-
氢氧化钠是重要的化工原料,其俗称是
A.纯碱 B.烧碱 C.小苏打 D.熟石灰
难度: 简单查看答案及解析
-
下列物质中,能用作钾肥的是
A.K2SO4 B.CO(NH2)2 C.NH4NO3 D.Ca(H2PO4)2
难度: 简单查看答案及解析
-
下列物质敞口放置,因发生化学变化质量增加的是
A.氢氧化钠 B.浓硫酸 C.浓盐酸 D.碳酸钙
难度: 中等查看答案及解析
-
次氯酸钠(NaClO)是某种家用消毒液的主要成分,其中氯元素的化合价为
A.+5 B.+3 C.+1 D.-1
难度: 中等查看答案及解析
-
小刚测定了下列4种日用品的PH,其中呈酸性的是
日用品 A. 洁厕灵 B. 洗涤灵 C. 洗发水 D. 消毒液
PH 1 7 9 12
难度: 中等查看答案及解析
-
下列物质性质的表述中,属于化学性质的是
A.氧气无色无味 B.铝呈银白色 C.蔗糖易溶于水 D.碳酸易分解
难度: 中等查看答案及解析
-
下列物质中,含有氧分子的是
A.O2 B.H2O C.CO2 D.H2O2
难度: 中等查看答案及解析
-
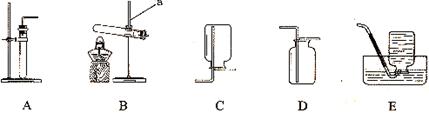
下列实验操作中,正确的是

A.倾倒液体 B.点燃酒精灯 C.取用固体粉末 D.过滤
难度: 简单查看答案及解析
-
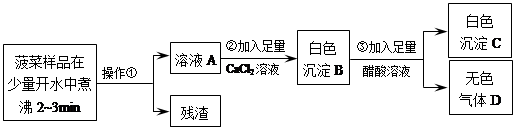
下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是
序号
实验目的
实验过程
①
证明变质
取少量溶液,滴加盐酸,将生成的气体通入石灰水
②
确定成分
取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液
③
测定纯度
取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量
④
除去杂质
取溶液,滴加石灰水至恰好完全反应,过滤
A.②③ B.①③ C.②④ D.①④
难度: 简单查看答案及解析
-
下列生活用品所使用的主要材料,属于有机合成材料的是

A.青花瓷瓶 B.塑料水杯 C.纯棉毛巾 D.不锈钢锅
难度: 简单查看答案及解析
-
能与无色硝酸银溶液反应,使溶液变为蓝色的金属是
A.铝 B.铁 C.铜 D.银
难度: 中等查看答案及解析
-
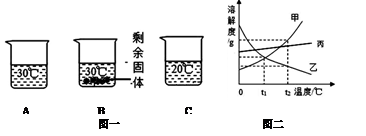
向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是
①
②
③
④
⑤
资料:A的溶解度
温度/℃
20
30
40
50
60
溶解度/g
37.2
41.4
45.8
50.4
55.2
A.②中A的质量分数最大
B.③⑤中A的质量分数相等
C.②④⑤的溶液为饱和溶液
D.①③④⑤中没有固体存在
难度: 中等查看答案及解析
-
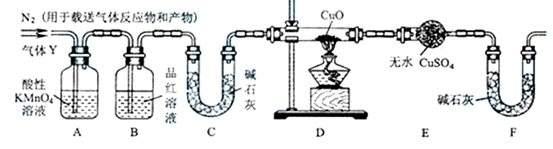
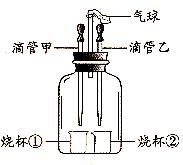
根据下图所示实验分析得出的结论中,不正确的是

难度: 中等查看答案及解析
-
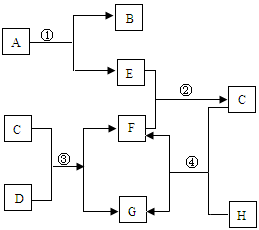
煤燃烧产生的废气中含有SO2,用NaOH、Na2SO3溶液可将90%以上的SO2吸收。涉及的反应有:
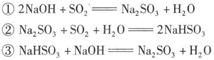
下列说法中,不正确的是:
A.反应②发生的是化合反应
B.可循环使用的物质是Na2SO3
C.NaHSO3中硫元素的化合价是+6
D.反应①说明SO2与CO2有相似的化学性质
难度: 简单查看答案及解析
-
生活中常有误食亚硝酸钠(NaNO2)中毒事件的报道,这是因为亚硝酸钠外观酷似食盐且有咸味;工业用盐中常混有亚硝酸钠,有关氯化钠和亚硝酸钠的部分资料如下表:
化学式
酸碱性
热稳定性
与稀盐酸的
反应现象
与硝酸银溶液的反应现象
氯化钠
中性
受热不分解
无明显变化
生成白色沉淀
亚硝酸钠
弱碱性
320℃以上会分解
放出刺激性气体
放出红棕色气体
无明显变化
如要检验食盐样品中有无亚硝酸钠,下列判定方法不正确的是
A.用pH试纸测定食盐样品溶液的酸碱性
B.取少量食盐样品加热到320℃以上,观察有无刺激性气体放出
C.取少量食盐样品,向其中加入盐酸,观察有无红棕色气体放出
D.取少量食盐样品加水溶解,加入硝酸银溶液观察有无白色沉淀
难度: 中等查看答案及解析
-
下列依据实验目的所设计的实验操作中,正确的是
选项 实验目的 实验操作
A 检验NaCl中含有Na2CO3 加水溶解
B 鉴别NaOH和Ca(OH)2溶液 加Na2CO3溶液
C 除去CaO中的CaCO3 加足量稀盐酸
D 除去CO2中的CO 通入足量NaOH溶液
难度: 中等查看答案及解析
-
工业上用甲和乙反应制备燃料丙。根据下列微观示意图得出的结论中,正确的是
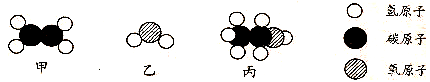
A. 甲的化学式为CH2 B. 反应中甲、乙、丙的分子个数比为2:1:1
C. 甲、乙、丙都是有机物 D. 丙中C、H、O元素的质量比为12:3:8
难度: 中等查看答案及解析
-
由C、H两种元素组成的化合物叫烃。常温常压下,分子中碳原子个数小于或等于4的烃通常为气体。常温常压下,C2H4和另一种烃组成的混合气体中碳元素的质量分数为87%,则混入的烃可能是
A.C8H8 B.C2H6 C.C2H2 D.CH4
难度: 中等查看答案及解析
-
下列四个图像能正确反映对应变化关系的是
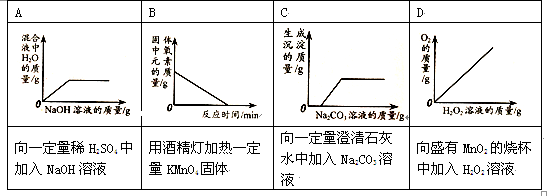
难度: 中等查看答案及解析