-
下列有关钢铁腐蚀与防护的说法正确的是( )
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷浓硝酸表面钝化,可保护内部不被腐蚀
C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe-3e-═Fe3+难度: 中等查看答案及解析
-
下列物质与常用危险化学品的类别不对应的是( )
A.H2SO4、NaOH--腐蚀品
B.CH4、C2H4--易燃液体
C.CaC2、Na--遇湿易燃物品
D.KMnO4、K2CrO7--氧化剂难度: 中等查看答案及解析
-
下列说法正确的是( )
A.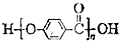 的结构中含有脂基
的结构中含有脂基
B.顺-2-丁烯和反-2-丁烯的加氢产物不同
C.1mol葡萄糖可水解生成2mol乳酸(C3H6O3)
D.脂肪和蛋白质都是能发生水解反应的高分子化合物难度: 中等查看答案及解析
-
用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合
理的是( )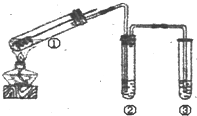
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证S02的生成
C.③中选用NaOH溶液吸收多余的S02
D.为确认CuS04生成,向①中加水,观察颜色难度: 中等查看答案及解析
-
下列解释实验事实的方程式不正确的是( )
A.0.1mol/LCH3COOH溶液的pH>1:CH3COOH⇌CH3COO-+H+
B.“NO2球”浸泡在冷水中,颜色变浅:2NO2(g)(红棕色)⇌N2O4(g)(无色)△H<0
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-⇌3Fe2++2NO2+4H2O
D.向Na2CO3溶液中滴入酚酞,溶液变红:CO32-+H2O⇌HCO3-+OH-难度: 中等查看答案及解析
-
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS).下列分析正确的是( )
A.CuS的溶解度大于PbS的溶解度
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-═CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应,然后硫酸铜与ZnS、PbS发生复分解反应生成更难溶的CuS难度: 中等查看答案及解析
-
某温度下,H2(g)+CO2(g)⇌H2O(g)+CO(g) 的平衡常数K=
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示.下列判断不正确的是( )
起始浓度 甲 乙 丙 c(H2)/mol/L 0.010 0.020 0.020 c(CO2)/mol/L 0.010 0.010 0.020
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢难度: 中等查看答案及解析
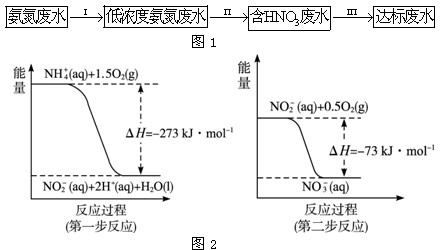
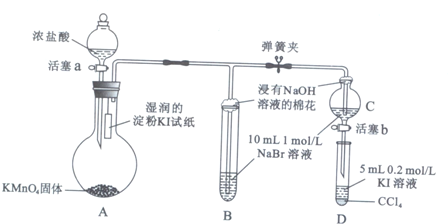
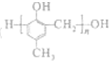 )的合成路线如图所示:①②
)的合成路线如图所示:①②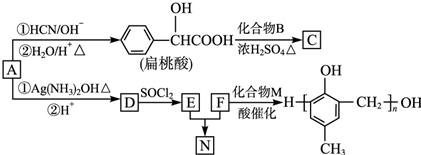
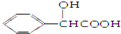 )有多种同分异构体.属于甲酸酯且含酚羟基的同分异构体共有______种,写出其中一种含亚甲基(-CH2-)的同分异构体的结构简式______.
)有多种同分异构体.属于甲酸酯且含酚羟基的同分异构体共有______种,写出其中一种含亚甲基(-CH2-)的同分异构体的结构简式______.