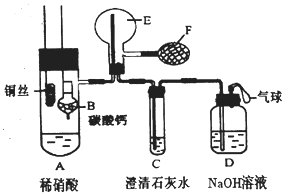
-
天然气燃烧过程中的能量转化方式为
A. 化学能转化为热能 B. 化学能转化为电能
C. 热能转化为化学能 D. 化学能转化为机械能
难度: 中等查看答案及解析
-
锗(Ge)是第四周期第ⅣA族元素,处于元素周期表中金属区与非金属区的交界线上,下列叙述正确的是
A. 锗是一种金属性很强的元素 B. 锗的单质具有半导体的性能
C. 锗化氢(GeH4)稳定性很强 D. 锗酸(H4GeO4)是难溶于水的强酸
难度: 中等查看答案及解析
-
在某罐头车的车身上印有如下图所示警示标记,则车内装的物品不可能为

A. 酒精 B. 浓硫酸 C. 浓氨水 D. 浓HNO3
难度: 简单查看答案及解析
-
已知氧元素的原子结构示意图为
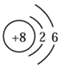 ,试推测其在元素周期表的位置为
,试推测其在元素周期表的位置为A. 第二周期IIA族 B. 第三周期IIA族
C. 第二周期VIA族 D. 第三周期VIA 族
难度: 简单查看答案及解析
-
如图所示是分离混合物时常用的仪器,从左至右,这些仪器可以进行混合物分离操作的名称分别是
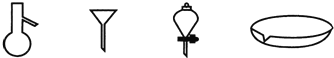
A.蒸馏、蒸发、萃取、过滤 B.萃取、过滤、蒸馏、蒸发
C.蒸馏、过滤、萃取、蒸发 D.过滤、蒸发、萃取、蒸馏
难度: 中等查看答案及解析
-
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作下列图示对应的操作规范的是( )
A. 称量
 B. 溶解
B. 溶解C. 转移
 D. 定容
D. 定容
难度: 简单查看答案及解析
-
从如图所示的两种微粒结构示意图中,不正确的是
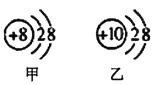
A. 它们的核外电子数相同 B. 它们属于同种元素
C. 甲表示阴离子,乙表示原子 D. 它们的核外电子层数相同
难度: 简单查看答案及解析
-
现有IL1.0mol/L 的氨水,下列关于该氨水的说法正确的是
A. NH3•H2O的物质的量为1mol B. NH4+为1mol
C. NH3、NH3•H2O、NH4+的物质的量之和为1mol D. NH3为1mol
难度: 简单查看答案及解析
-
同一周期X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性是: HXO4>H2YO4>H3ZO4,则下列判断错误的是
A. 原子半径:X > Y > Z B. 气态氢化物的稳定性:HX > H2Y > ZH3
C. 非金属性:X > Y > Z D. 阴离子的还原性:Z3-> Y2-> X-
难度: 中等查看答案及解析
-
某一K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.5 mol/L,SO42-的物质的量浓度为0.8 mol/L,则此溶液中K+的物质的量浓度为( )
A. 0.1 mol/L B. 0.15 mol/L
C. 0.2 mol/L D. 0.25 mol/L
难度: 中等查看答案及解析
-
反应2SO2+O2
2SO3达到平衡状态后,下列说法正确的是
A. 三氧化硫的生成速率与分解速率相等
B. 二氧化硫、氧气、三氧化硫的分子数之比是2:1:2
C. 二氧化硫与氧气不再化合生成三氧化硫
D. 降低温度,原化学平衡状态未被破坏
难度: 简单查看答案及解析
-
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是
A. 元素非金属性技X、Y、Z的顺序减弱
B. 阴离子的还原性按X、Y、Z的顺序减弱
C. 气态氢化物的稳定性按X、Y、Z的顺序增强
D. 单质的氧化性按X、Y、Z的顺序增强
难度: 简单查看答案及解析
-
含硒(Se) 的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是
A. 非金属性比硫强 B. 氢化物比HBr稳定
C. 原子序数为34 D. 最高价氧化物的水化物显碱性
难度: 中等查看答案及解析
-
甲、乙是周期表中相邻同主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A. x+2 B. x +4 C. x+8 D. x+18
难度: 中等查看答案及解析
-
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wu thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )
A. 13C与15N有相同的中子数
B. 13C与C60互为同素异形体
C. 15N与14N互为同位素
D. 15N的核外电子数与中子数相同
难度: 中等查看答案及解析