-
下列离子方程式表达正确的是( )
A.SO2通入溴水中:SO2+2H2O+Br2=2H++SO42-+2HBr
B.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
C.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.4.6g乙醇中含有的C-H键的个数为0.6NA
B.34g H2O2中含有的阴离子数为NA
C.标准状况下,11.2L CHCl3中含有的分子数为0.5NA
D.常温常压下,21g氧气和27g臭氧中含有的氧原子总数为3NA难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl-
B.使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-
C.含有大量ClO-的溶液中:K+、OH-、I-、SO32-
D.c(Al3+)=0.1mol•L-1的溶液中:Na+、Cl-、AlO2-、SO42-难度: 中等查看答案及解析
-
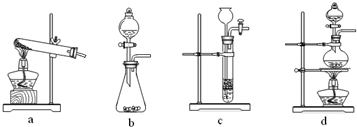
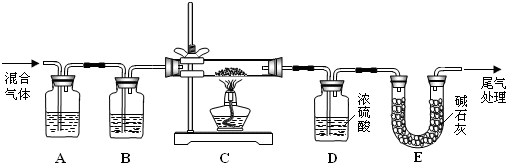
下列有关实验原理或操作正确的是( )
A.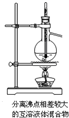
B.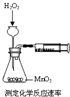
C.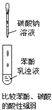
D.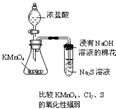
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
B.使用催化剂可以改变化学反应的反应热
C.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠
D.反应2CO(g)=2C(s)+O2(g)△H>0可以自发进行难度: 中等查看答案及解析
-
向含Na2CO3、Na[Al(OH)4]的混合溶液中逐滴加入150mL 1mol•L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )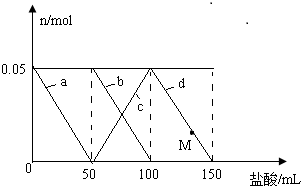
A.a曲线表示的离子方程式为:[Al(OH)4]-+H+=Al(OH)3↓+H2O
B.b和c曲线表示的离子反应是相同的
C.M点时,溶液中沉淀的质量为3.9g
D.原混合溶液中的CO32-与[Al(OH)4]-的物质的量之比为1:2难度: 中等查看答案及解析
-
短周期主族元素A、B、C、D的原子序数依次增大,A、B、C原子的最外层电子数之和为12,B、C、D位于同一周期,C原子的最外层电子数既是A原子内层电子数的3倍又是B原子最外层电子数的3倍.下列说法正确的是( )
A.元素A、C的最高价氧化物对应的水化物都是弱酸
B.元素B能与A的最高价氧化物发生置换反应
C.元素B和D能形成BD2型的共价化合物
D.D的单质有毒,且有漂白性难度: 中等查看答案及解析