-
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各为1.5mol,Mg2+为0.5mol,则SO42-的物质的量为( )
A.0.1mol
B.0.5mol
C.0.15mol
D.0.25mol难度: 中等查看答案及解析
-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液难度: 中等查看答案及解析
-
离子方程式H++OH-=H2O可表示的化学反应是( )
A.盐酸和氢氧化钡的反应
B.硝酸和氢氧化镁的反应
C.硫酸和氢氧化钡的反应
D.盐酸和氢氧化铜反应难度: 中等查看答案及解析
-
胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.产生丁达尔现象
C.分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在难度: 中等查看答案及解析
-
下列溶液中Cl-浓度与50mL 1mol•L-1 AlCl3溶液中Cl-浓度相等的是( )
A.150mL 1mol•L-1的NaCl溶液
B.75mL 2mol•L-1NH4Cl溶液
C.150mL 2mol•L-1的KCl溶液
D.75mL 1mol•L-1的FeCl3溶液难度: 中等查看答案及解析
-
在同一稀溶液中可以共存,加OH-有沉淀生成,加H+有气体生成的一组是( )
A.Mg2+、CO32-、Cu2+、Cl-
B.HCO3-、Cl-、Ca2+、Mg2+
C.OH-、NO3-、K+、Ca2+
D.SO42-、H+、Al3+、NH4+难度: 中等查看答案及解析
-
下列离子方程式的表达正确的是( )
A.CuSO4溶液与Ba(OH)2溶液混合:Ba2++SO42-=BaSO4↓
B.NaHCO3溶液与稀硫酸混合:HCO3-+H+=H2O+CO2↑
C.NaHSO3溶液与NaHSO4溶液混合:HSO3-+HSO4-=SO42-+H2O+SO2↑
D.Ca(OH)2溶液中通入过量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O难度: 中等查看答案及解析
-
某实验小组只领取下列仪器或用品:铁架台、铁圈、铁夹、三角架、石棉网、烧杯、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、蒸馏烧瓶、火柴、滤纸、漏斗.只应用上述仪器或用品,不能进行的实验操作是( )
A.蒸发
B.萃取
C.过滤
D.蒸馏难度: 中等查看答案及解析
-
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列叙述不正确的是( )
A.NaCl的摩尔质量是58.5g/mol
B.将wga%的NaCl溶液蒸发掉g水,得到2a%的NaCl溶液
C.将1体积cmol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2cmol/L
D.将5.85gNaCl晶体溶入1000mL水中,制得0.1mol/L的NaCl溶液难度: 中等查看答案及解析
-
下列物质混合发生化学反应,且反应属于离子反应的是( )
A.H2和O2反应生成水
B.锌片投入稀硫酸中
C.KClO3(固体)和MnO2(固体)混合加热制O2
D.NaOH溶液和K2SO4溶液混合难度: 中等查看答案及解析
-
等质量的CH4和NH3相比较,下列结论错误的是( )
A.它们的分子个数比为17:16
B.它们的原子个数比为17:16
C.它们的氢原子个数比为17:12
D.它们所含氢元素的质量比为17:12难度: 中等查看答案及解析
-
某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡没亮,但是按照图乙接好路线,灯泡亮了.由此得出的以下结论中正确的是( )
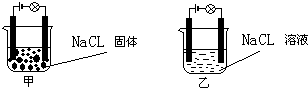
A.NaCl是非电解质
B.NaCl溶液是电解质
C.在NaCl溶液中,水电离出了大量的离子
D.NaCl在水溶液中电离出了可以自由移动的离子难度: 中等查看答案及解析
-
某地有甲、乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、CO32-、NO3-、OH-.若两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清只含硝酸钠而排放,污染程度会大大降低.关于污染源的分析,你认为正确的是( )
A.CO32-和NO3-可能来自同一工厂
B.Na+和NO3-来自同一工厂
C.Ag+和Na+可能来自同一工厂
D.Cl-和NO3-一定不在同一工厂难度: 中等查看答案及解析
-
不用其它试剂,用最简便的方法鉴别:①Ba(OH)2 ②HNO3 ③Na2SO4 ④CuCl2四种溶液,鉴别出的先后顺序是( )
A.④①③②
B.④②③①
C.③②④①
D.②③①④难度: 中等查看答案及解析
-
在电解质溶液中,下列叙述正确的是( )
A.阳离子和阴离子数目一定相等
B.阳离子带的正电荷总数一定和阴离子带的负电荷总数相等
C.除阴、阳离子外,溶液中不会再有其他微粒
D.能导电是因为与外界通电难度: 中等查看答案及解析
-
在无色透明酸性溶液中,能共存的离子组是( )
A.NH4+、NO3-、Al3+、Cl-
B.K+、SO42-、HCO3-、Na+
C.Cu2+、NO3-、Cl-、Na+
D.MnO4-、K+、SO42-、Na+难度: 中等查看答案及解析
-
下列实验装置与实验操作正确的是( )
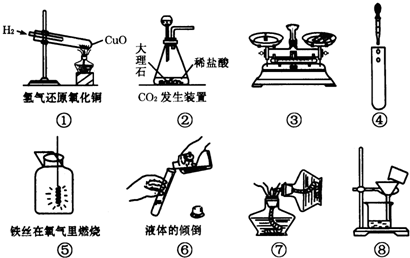
A.①④⑤
B.②③⑧
C.④⑥
D.⑤⑦难度: 中等查看答案及解析
-
下列不存在丁达尔效应的分散系是( )
A.有尘埃的空气
B.纯水
C.溴水
D.向沸水中滴入FeCl3饱和溶液所得液体难度: 中等查看答案及解析
-
下列事实不能用胶体的知识来解释的是( )
A.用某些含铝的化合物作净水剂
B.医学上利用用透析的手段净化尿毒症患者的血液
C.用一束平行光线照射蛋白质溶液时,从侧面看可看到光亮的通路
D.向FeCl3溶液中滴入NaOH溶液,出现红褐色沉淀难度: 中等查看答案及解析
