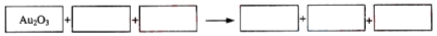-
下列有关金属及其合金的说法不正确的是
A.目前我国流通的硬币是由合金材料制造的
B.生铁、普通钢和不锈钢中的碳含量依次增加
C.镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
难度: 简单查看答案及解析
-
氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过反应:Al2O3+N2+3C
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮的化合价为+3
D.AlN的摩尔质量为41 g
难度: 简单查看答案及解析
-
钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2;
②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。
下列
说法正确的是
A.反应①、②中电子转移数目相等
B.反应①中氧化剂是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
难度: 简单查看答案及解析
-
下列叙述正确的是
A.48gO3气体含有6.02×1023个O3分子
B.常温常压下,4.6gNO2气体含有1.81×1023个
NO2分子
C.0.5mol·L-1CuCl2溶液中含有3.01×1023个Cu2+
D.标准状况下,33.6LH2O含有9.03×1023个H2O分子
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1mol任何气体所占的体积为22.4L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
难度: 中等查看答案及解析
-
有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl
离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为( )
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a D.(2y-4x)/a
难度: 中等查看答案及解析
-
将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为
A.NO2 B.N2O2 C.N2O D.N2O4
难度: 简单查看答案及解析
-
能正确表示下列反应的离子方程式是
A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO—+CO2+H2O =CaCO3↓+2HClO
B.向次氯酸钙溶液通入SO2:Ca2++2ClO—+SO2+H2O= CaSO3↓+2HClO
C.氢氧
化钙溶液与碳酸氢镁溶液反应:HCO3—+Ca2++OH—=CaCO3↓+H2O
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3—=3Fe
3++NO↑+2H2O
难度: 简单查看答案及解析
-
下列各组离子一定能大量共存的是
A.在含有大量[Al(OH)4]- 溶液中NH4+、Na+、Cl-、H+
B.在强碱溶液中 Na+、K+、CO32-、NO3-
C.在pH=12的溶液中 NH4+、Na+、SO42-、Cl-
D.在c(H+)=0.1 mol·L-1的溶液中K+、I-、Cl-、NO3-
难度: 简单查看答案及解析
-
下列实验可行的是
A.用澄清石灰水检验CO中含有的CO2
B.用BaCl2除去NaOH溶液中混有的少量Na2SO4
C.用KSCN溶液检验溶液中含有的Fe2+
D.用溶解、过滤的方法分离CaCl2和NaCl固体混合物
难度: 简单查看答案及解析
-
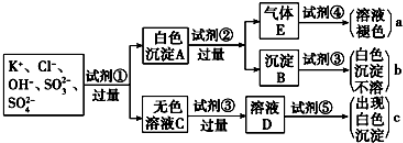
某溶液中可能含有SO42-、CO32-、Cl-。为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是
A.H2SO4 B.HCl C.NaOH D.NaNO3
难度: 简单查看答案及解析
-
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
难度: 简单查看答案及解析
-
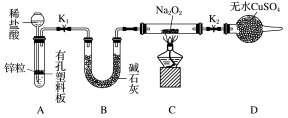
从绿色化学的理
念出发,下列实验不宜用图7所示装置进行的是

A.不同浓度的硝酸与铜的反应
B.稀硫酸与纯碱或小苏打反应
C.铝与氢氧化钠溶液或稀盐酸反应
D.H2O2在不同催化剂作用下分解
难度: 简单查看答案及解析
-
下列做法中不符合“绿色化学”思想的是
A.以水性涂料代替油性涂料
B.以无磷洗涤剂代替含磷洗涤剂
C.试验后的有毒有害物质应分类收集,统一处理
D.在通风橱中制取氯气时不用NaOH溶液吸收尾气
难度: 简单查看答案及解析
-
下列有关物质分类一定正确的是( )
A.强电解质:盐酸、氢氧化钡、明矾
B.弱电解质:甲酸、纯碱、醋酸铵
C.非电解质:液氨、二氧化硫、苯
D.同系物:CH2O2、C2H4O2、C3H6O2
难度: 简单查看答案及解析
-
下列有关金属铝及其化合物的叙述正确的是
A.铝在常温下不能与氧气反应 B.铝不能与氯气反应
C.铝既能溶于酸,又能溶于碱 D.氧化铝只能与酸反应,不能与碱反应
难度: 简单查看答案及解析
-
下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
难度: 简单查看答案及解析
-
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.密闭容器中CuO和C高温反应的气体产物:
B.Fe在Cl2中的燃烧产物:
C.AlCl3溶液中滴加NaOH后铝的存在形式:
D.
氨水与SO2反应后溶液中的铵盐:
难度: 中等查看答案及解析
-
能实现下列物质间直接转化的元素是
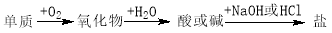
A.硅 B.硫 C.铜 D.铁
难度: 简单查看答案及解析
-
下列实验能达到实验目的且符合安全要求的是
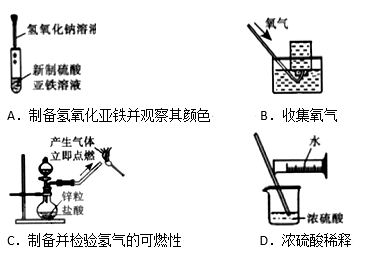
难度: 简单查看答案及解析
-
若20 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有2 g Ca(NO3)2,则溶液中NO
的物质的量浓度为( )
A.
mol·L-1 B.
mol·L-1 C.
mol·L-1 D.
mol·L-1
难度: 简单查看答案及解析
-
有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025 mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D.Fe5O7
难度: 简单查看答案及解析
-
向含2 mol NaOH、1 mol Ba(OH)2、2 mol Na[Al(OH)4]的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量的关系不正确的是( )
选项
A
B
C
D
n(CO2)(mol)
2
3
4
6
n(沉淀)(mol)
1
2
3
2
难度: 中等查看答案及解析
-
已知四种盐的溶解度(S)曲线如下图所示,下列说法不正确的是( )
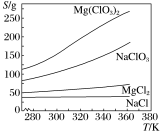
A.将NaCl溶液蒸干可得NaCl固体
B.将MgCl2溶液蒸干可得MgCl2固体
C.Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯
D.可用MgCl2和NaClO3制备Mg(ClO3)2
难度: 困难查看答案及解析
-
在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是( )
A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+
B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+
D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
难度: 中等查看答案及解析