-
2014年2月22日是第35个“世界地球日”,我国确定的主题是“善待地球——科学发展”。下列行为中不符合这一主题的是( )
A.采用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.减少直至不使用对大气臭氧层起破坏作用的氟氯烃
C.大量开采地下水,以满足社会对水的需求
D.节约能源,提高能源利用率
难度: 简单查看答案及解析
-
下列说法正确的是 ( )
A.无氧酸是指分子组成中不含氧元素的酸,如HCl、CH4等
B.根据溶解性的不同,可将碱分为难溶性碱和可溶性碱
C.和酸反应生成盐和水的物质一定是碱性氧化物
D.所有的酸性氧化物都可以与水化合得到相应的酸
难度: 简单查看答案及解析
-
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后( )
A.上层为无色,下层为紫红色 B.整个溶液变为棕黄色
C.整个溶液变紫色 D.下层无色,上层紫红色
难度: 简单查看答案及解析
-
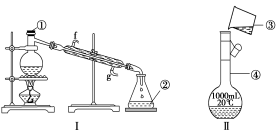
下列有关实验操作中,正确的是( )
A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,把过量的试剂倒入试剂瓶中
B.Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C.用蒸发的方法使NaCl从水溶液中析出时,应将蒸发皿中NaCl溶液全部蒸干
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后应冷却至室温才能转移到容量瓶中
难度: 中等查看答案及解析
-
提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
难度: 简单查看答案及解析
-
下列所含分子数由多到少的排列顺序是( )
① 标准状况下33.6LH2 ②所含电子的物质的量为4mol的H2 ③20℃.45gH2O
④常温下,16gO2,与14gN2的混合气体 ⑤含原子总数约为1.204×1024的NH3
A.③②①④⑤ B.①②③④⑤ C.③②⑤①④ D.②③①④⑤
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
C.在常温常压下,11.2 L Cl2含有的分子数为0.5 NA
D.标准状况下,11.2 L乙醇含有的分子数为0.5 NA
难度: 中等查看答案及解析
-
下列溶液中Cl-的物质的量浓度最大的是( )
A.200mL 2mol/L MgCl2溶液 B.1000mL 2.5mol/L NaCl溶液
C.250mL 1mol/L AlCl3溶液 D.300mL 5mol/L KClO3溶液
难度: 简单查看答案及解析
-
某溶液中含有较大量的Cl-、CO32-、OH- 3种阴离子,如果只取一次该溶液能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加过量Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加过量Ba(NO3)2溶液
A.①②④②③ B、④②①②③ C、①②③②④ D、④②③②①
难度: 中等查看答案及解析
-
在20g密度为dg/cm3的硝酸钙溶液里含1g Ca2+,则NO3-离子的物质的量浓度是( )
A.
mol·L-1 B.
mol·L-1 C.2.5d mol·L-1 D.1.25 d mol·L-1
难度: 中等查看答案及解析
-
在相同的温度和压强下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是a.CO2,100 mL;b.O2,200 mL;c.N2,400 mL;d.CH4,600 mL,则4个容器中气体的质量由大到小的顺序是( )
A.a>b>c>d B.b>a>d>c C.c>d>b>a D.d>c>a>b
难度: 中等查看答案及解析
-
标准状况下,m g A气体与n g B气体分子数相等,下列说法不正确的是( )
A. 标准状况下,同体积的气体A和气体B的质量比为m∶n
B. 25 ℃时,1 kg气体A与1 kg气体B的分子数之比为n∶m
C. 同温同压下,气体A与气体B的密度之比为m∶n
D. 标准状况下,等质量的A与B的体积比为m∶n
难度: 中等查看答案及解析
-
某溶液中大量存在以下五种离子:NO
、SO
、Fe3+、H+、M,其物质的量之比为n(NO
)∶n(SO
)∶n(Fe3+)∶n(H+)∶n(M)=2∶3∶1∶3∶1,则M可能为( )
A. Fe2+ B. Mg2+ C. CO
D. Ba2+
难度: 中等查看答案及解析
-
质量分数为a%,物质的量浓度为c mol·L-1的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为( )
A. 等于2c mol·L-1 B. 大于2c mol·L-1
C. 小于2c mol·L-1 D. 在c~2c mol·L-1之间
难度: 中等查看答案及解析
-
混合气体由N2和CH4组成,测得混合气体在标准状况下的密度为0.821g/L,则混合气体中N2和CH4的体积之比为( )
A.1:1 B.1:4 C.4:1 D.1:2
难度: 中等查看答案及解析